COVID-19相关肺毛霉菌病(CAPM)是一种罕见但被低估的 COVID-19 并发症。目前, CAPM仍未得到充分诊断。一篇发表在Lancet Infect Dis上的共识对CAPM的定义、诊断和管理进行了建议。内容总结如下。
一、CAPM的定义
CAPM定义为与COVID-19同时或在COVID-19确诊后的3个月内确诊的肺毛霉菌病,并进一步分为确诊、临床诊断和拟诊三个层级。
表1 CAPM的定义
| 确诊CAPM | 组织病理学或细胞学显示无菌菌丝或通过无菌程序从无菌的部位(胸膜液或肺)获得的培养物显示毛霉生长。 |
| 临床诊断CAPM | 包括:兼有CAPM和 COVID-19 相关的肺曲霉病(CAPA ) 的临床特征、危险因素、影像学提示CAPM(厚壁空洞、大面积实变、反晕征(RHS) 或多个大结节)、无隔菌丝的证据(有或没有毛霉生长)和代表下呼吸道的样本(包括支气管肺泡灌洗液、非支气管镜支气管灌洗液、支气管冲洗液、支气管刷检洗液、气管内分泌物和痰液)。 |
| 拟诊CAPM | 包括:兼有临床特征;未经控制的糖尿病、过度或不恰当的糖皮质激素治疗(剂量、持续时间或现有COVID-19中的循证证据不支持用于其他适应症);在没有其他明确诊断的情况下,影像学检查高度怀疑CAPM(反晕征、真菌性动脉瘤或厚壁腔)。 |
二、流行病学特征
据报道,社区 COVID-19 患者的 CAPM 患病率为 0.01%(数据来自墨西哥的一个中心),COVID-19 住院患者的 CAPM 患病率为 0.15%(数据来自五个三级医疗机构)。一项系统性评价结果显示,在全球接受调查的275例患者中,有CAPM患者26例(9.5%)。印度报告的 233 例 COVID-19 相关毛霉菌病 (CAM) 病例中有 17 例 (7.3%) 和世界其他地区报告的 42 例 CAM 病例中有 9 例 (21.4%) 是由 CAPM 引起的。CAPM 的汇总患病率估计为每 10 000 例因 COVID-19 入院的患者中有 5例(95% CI < -29)。
三、危险因素
未经控制的糖尿病(或高血糖)和不恰当(过度)的糖皮质激素治疗是发生CAPM的主要危险因素,COVID-19本身和其相关的铁代谢失调也是影响CAPM发生的因素。
四、临床特点
尚未发现CAPM的特异性临床特征,无法通过临床表现来区分CAPM和COVID-19和其他肺炎。当COVID-19患者的痰呈褐色或黑色同时伴有咯血症状,尤其是对存在上述危险因素的患者,应进行CAPM相关检查。其他提示CAPM的临床表现包括胸痛,抗生素治疗≥8小时仍发热,咳嗽加重或咳痰,空洞,或在相关情况(例未经控制的糖尿病)下肺部X片示肺泡阴影加重。
五、对疑似CAPM的评估
CT的诊断效能优于胸部X射线检查。在符合影像学特点的前提下,从痰液或气管内分泌物中分离出毛霉菌表示该患者可能患有毛霉菌病。痰液检查是一种非侵入性检查方法,可以用作初筛。使用支气管镜检查获得的呼吸道样本的诊断率可能更高。尚无针对毛霉菌病的特异性血清学标志物。专家组推荐使用增强CT扫描和下呼吸道样本的常规微生物检测作为诊断CAPM的第一步(共识水平:100%)。
六、CAPM的影像学检查
连续的影像学检查有助于鉴别COVID-19和CAPM。因COVID-19出现的晕轮征和RHS往往会随着时间的推移而改善,而在肺毛霉菌病中,常见的过程是形成空洞。因此,时间、临床情况(未经控制的糖尿病、持续或新发发热、咯血或咳痰),以及病程有助于鉴别急性COVID-19和CAPM。
CAPM的影像学特征分为4类:高度怀疑、怀疑、非特异性或排除CAPM。与存在多个结节(患有血液肿瘤的肺毛霉菌病患者中)相比,存在厚壁空洞、鸟巢征、RHS和其他特征被认为是高度怀疑CAPM的特征。真菌性动脉瘤患者可能需要进行数字减影血管造影。
表2 CAPM的影像学特征
|
高度怀疑 •厚壁空洞 •反晕征 •大面积实变或坏死性肺炎 •霉菌性动脉瘤 •鸟巢征 •多个大结节(结节>1cm) •连续成像显示具有气液平面的空洞 |
|
怀疑 •胸腔积液 |
|
非特异性的 •气胸 |
|
不怀疑 •纵隔淋巴结肿大 •小叶中心结节或树芽征(可见于咯血患者或同时存在COVID-19相关肺曲霉病患者) |
在适当的临床情况下,存在RHS、厚壁空洞、鸟巢征、真菌性动脉瘤、大面积实变或坏死性肺炎,以及多个大结节(>1cm)和连续成像显示具有气液平面的空洞,这些都是高度怀疑CAPM的影像学特征(共识水平:72-100%)。不建议对CAPM患者进行鼻旁窦或大脑的常规影像学检查(共识水平:89%)。
七、支气管镜检查
在遵守标准预防措施的情况下,可随时对COVID-19患者进行可曲式支气管镜检查。即使是在因COVID-19引起的严重急性呼吸窘迫综合征的患者中,也可安全地使用60mL盐水进行支气管镜检查和支气管肺泡灌洗(吸入空气的氧分压中位数为0.8,呼气末正压为10cm水)。
推荐对大多数CAPM患者进行早期软支气管镜检查(共识水平:95%),优点:气道病变可视化、进行支气管内膜活检以及提供可以代表下呼吸道的样本(支气管肺泡灌洗液或支气管冲洗液)。
八、经胸壁肺活检和细针穿刺
通过电视胸腔镜手术或开胸手术取样的活检可能会确定对疑似CAPM患者的诊断。然而,考虑到疑似CAPM患者可能发生严重出血,在进行空心针活检之前,可以考虑通过现场细胞病理学检查进行细针穿刺细胞学检查。
推荐经胸空心针活检用于有外周肺病变CAPM患者的诊断(共识水平:91%)。
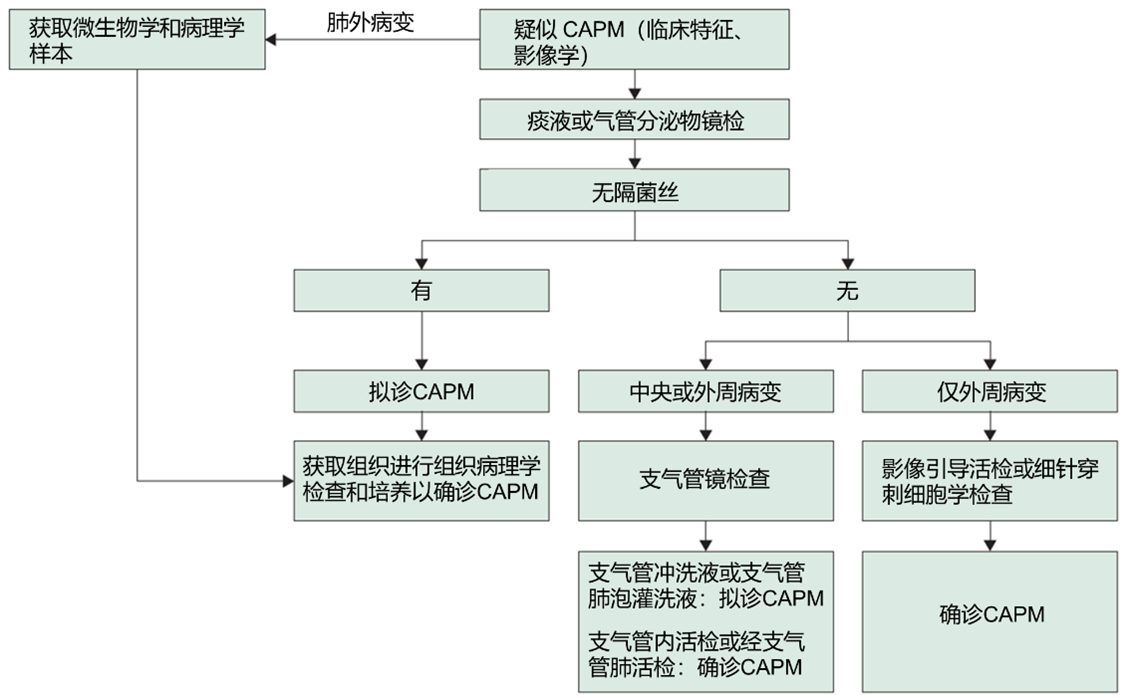
图1 疑似CAPM患者的诊断流程
九、临床生物样本的质量和样本处理的技术细节
专家认为直接显微镜检查比进行样本培养更可靠。在临床影像学高度怀疑的情况下,仅毛霉菌生长(尽管直接涂片镜检阴性)代表临床诊断为CAPM。
十、核酸扩增检测
核酸扩增 (NAA)检测对血液或体液的诊断作用仍不清楚,专家不建议常规使用NAA检测来诊断CAPM。从无菌环境取样的毛霉菌NAA检测为CAPM提供了支持性证据。专家组建议使用标准化NAA方法对无菌样本或支气管肺泡灌洗液进行检测(共识水平:74%)。
十一、毛霉菌鉴定和药敏试验
专家组推荐对毛霉种类进行鉴定和进行抗真菌药敏试验,以指导选择抗真菌药,同时在疾病进展的患者中进行上述两项试验(共识水平:71-74%)。
十二、CAPM的组织病理学特征
目前尚不清楚CAPM的组织病理学与非CAPM是否有差异。有限的经验表明真菌对组织的影响几乎没有差异。在接受CAPM手术的患者的病理标本中也发现了曲霉菌和毛霉菌的双重感染,使用抗根霉属(和其他毛霉)抗体的免疫组化法有助于区分二者。在复杂病例中,也可以尝试通过PCR(和DNA测序)在新鲜组织或福尔马林固定的石蜡包埋组织中鉴定毛霉菌DNA。
十三、CAPA和CAPM双重感染
由于相同的危险因素和相似的临床影像学特征,在鉴别诊断中,CAPA与CAPM的特点最相近。CAPA和CAPM双重感染进一步增加了诊断难度。虽然糖皮质激素是CAPA和CAPM的危险因素,但控制不佳的糖尿病与CAPM的相关性更高。
CAPM的影像学特点与CAPA有相同之处。侵袭性肺曲霉病患者胸部增强CT可见血管闭塞征(侵犯血管导致),肺毛霉菌病患者中也有上述表现。鸟巢征见于多达1/3的肺毛霉菌病患者,而侵袭性肺曲霉病患者的这一比例为3%,这可能有助于区分两种侵袭性霉菌感染。
支气管肺泡灌洗液β-D-葡聚糖和半乳甘露聚糖阴性的患者诊断为CAPM的概率更高。诊断时可能会遇到多种提示双重感染的情况。
十四、CAPM的预防
预防CAPM最重要的一步是适当地使用糖皮质激素和其他COVID-19免疫抑制剂。糖皮质激素应仅用于COVID-19低氧血症患者,使用剂量和持续时间符合当前指南。专家小组建议不要使用抗真菌药物预防COVID-19患者的CAM或CAPM。相反,重点是将血糖控制在最佳状态。
十五、控制潜在的危险因素
与其他重症患者一样,建议对 CAPM患者进行严格的血糖控制(7.8–10.0 mmol/L)。在移植患者开始或停用其他免疫抑制之前,必须权衡风险-获益比。一般对于使用免疫抑制的移植受者,发生CAPM可继续使用低剂量糖皮质激素以避免移植排斥。
十六、CAPM的治疗
手术
CAPM-GG建议对所有有潜在可切除病灶的患者进行手术。
药物治疗
建议将CAPM的治疗分为初始治疗和维持治疗两个阶段。具体的治疗建议可参见指南共识原文。
参考文献:
- Muthu V, Agarwal R, Patel A, et al. Definition, diagnosis, and management of COVID-19-associated pulmonary mucormycosis: Delphi consensus statement from the Fungal Infection Study Forum and Academy of Pulmonary Sciences, India [published online ahead of print, 2022 Apr 4] [published correction appears in Lancet Infect Dis. 2022 Apr 14;:]. Lancet Infect Dis. 2022;S1473-3099(22)00124-4. doi:10.1016/S1473-3099(22)00124-4



