
乳腺癌是女性最常见且具有异质性的恶性肿瘤疾病,其相关治疗决策受组织病理学结果影响[1],而人表皮生长因子受体 2(HER2)是影响治疗决策的重要生物标志物[2]。在临床实践中,超过半数患者表现为 HER2 低表达乳腺癌,而最近新型疗法出现,为 HER2 低表达乳腺癌患者带来新的希望[3]。但直到目前,学术界对 HER2 低表达乳腺癌临床诊疗中面临的一些问题尚存争议。在此,本文总结 HER2 低表达乳腺肿瘤的特征及治疗进展,并梳理当前学术界争议要点、面临的挑战以及未来发展方向,以供广大医务工作者查阅参考。
一. HER2低表达乳腺肿瘤的定义
在传统认知中,乳腺肿瘤可根据免疫组织化学染色法(IHC)检测的 HER2 表达情况分为两类:
- HER2+:IHC3+或 IHC2+/原位杂交技术(ISH)检测显示 HER2 相关基因扩增
- HER2-:IHC0、IHC1+或 IHC2+/ISH 检测显示无 HER2 相关基因扩增。
推动 ASCO-CAP 重新审视 HER2 诊断标准的动力是 2022 年发布的 DESTINY-Breast04 研究的结果[ASCO-CAP 2023, DB042022]。这是一项开放标签 III 期研究,入组人群为 HER2 IHC 结果为+/2+且 ISH 未扩增的乳腺癌患者,这些患者在后线接受了 ADC 药物德曲妥珠单抗(T-Dxd)与医生选择的化疗方案的对比治疗。研究方案中使用“HER-2 低表达”作为 IHC+/2+且 ISH 未扩增的简称。研究结果表明,这类患者可从 T-Dxd 治疗中获益。这些发现挑战了对 HER-2 诊断的传统观点,从 HER-2 阴性中拆分出了 HER-2 低表达的人群。而 2024 年发布的 DESTINY-Breast06 研究[DB-06]将入组人群进一步扩展至 HER-2 超低表达的乳腺癌患者,结果显示 HER-2 低表达及超低表达人群的 PFS 获益显著。DB-06 的研究成果的公布,将 T-Dxd 的治疗获益人群进一步拓展至 HER2 超低表达。基于这项研究结果,NCCN 2025 V1[NCCN 2025 V1]版中对 HER2 检测部分进行了修改更新,HER2 IHC 0(无膜染色)与 IHC 0+(≤10%的细胞呈现微弱的、不完整的膜染色)、1+、2+/ISH-结果二点区分(无论是原发性还是转移性标本中)具有临床意义。
在未来,HER2 相关分类法可能会进一步细化(见图 1)[2]。
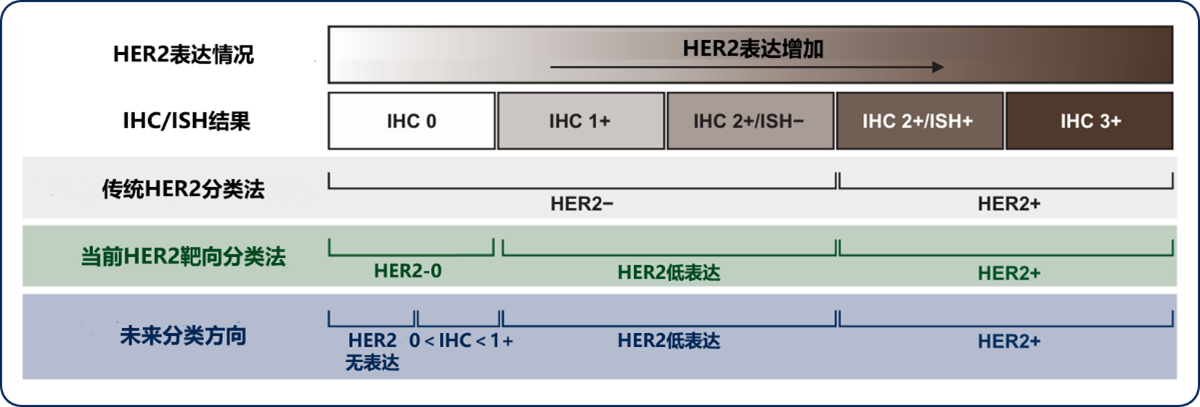
图片改编自:Open questions, current challenges, and future perspectives in targeting human epidermal growth factor receptor 2-low breast cancer. Fig 1.
HER2:人表皮生长因子受体 2;IHC:免疫组织化学染色法;ISH:原位杂交技术
图 1 乳腺肿瘤根据HER2表达情况分类法的演变与未来方向[2]
二. HER2低表达乳腺肿瘤的相关特征
随着检测结果进一步细化,随之而来的问题之一是,HER2 低表达/超低表达是否能成为独立亚型?为了回答这个问题,需要明确 HER2 低表达患者临床病理和分子特征及预后的影响。
1. HER2 低表达乳腺肿瘤的临床病理特征
在乳腺肿瘤中,HER2 低表达情况可发生于 46%~85%的激素受体阳性(HR+)肿瘤以及 32%~63%的三阴性乳腺癌(TNBC)中,此类肿瘤在大小和淋巴结形态上与 HER2-0 表型肿瘤存在差异[2]。多数研究表明,相较于 HER2-0 表型肿瘤而言,HER2 低表达肿瘤中表达 HR+的几率更高,但肿瘤的组织学分级、细胞核型分级和 Ki-67(由基因 MKI67 编码的一种反映细胞增殖情况的标志物)标记指数则相对较低[4]。另有研究显示:HER2 低表达肿瘤比例随雌激素受体(ER)表达阈值升高而逐渐增加。这些发现表明 HR 表达状态与 HER2 低表达乳腺肿瘤的生物学特征显著相关[4]。
2. HER2低表达乳腺肿瘤的分子特征
在分子特征方面,相关权威共识不认为 HER2 低表达乳腺肿瘤是一个独特的表型,而是将其视为一组多样化的肿瘤,此类肿瘤的生物学特性取决于肿瘤 HR 的表达情况[4],这一观点有多项研究结果佐证。
从内源亚型角度看,HER低表达肿瘤的亚型分布差异与 HR 表达情况相关。一项 HER2 低表达肿瘤 PAM50*分析相关研究显示,HER2 低表达肿瘤中 Luminal A 型及 Luminal B 型特征表达上调,而 HER2 富集型、基底细胞型及正常型的相关特征表达下调。该研究的 HR 亚组分析显示,HR+亚组结果与总体样本结果相似,但在 HR-(即 TNBC)组中则未观察到这种差异。另有一项研究也显示,HR+HER2 低表达肿瘤在内源亚型层面的分布情况与 HR+HER2-0 肿瘤相似,而与 TNBC 不同[4]。
深入到基因表达层面。目前已观察到 HER2 低表达肿瘤和 HER2-0 肿瘤间 PAM50 相关内源亚型差异相关的基因组改变,但这种差异同样很大程度上取决于 HR 表达情况。例如当合并 HR 亚组分析时,HER2 低表达肿瘤更可能出现 PIK3CA(编码磷脂酰肌醇相关激酶催化亚基的基因)突变,TP53(编码细胞周期调控相关蛋白 p53 的基因)突变则少见。但在单独分析HR亚组时却未观察到 PIK3CA 突变率的差异,而是仅在 HR+肿瘤中观察到 TP53 突变率的差异[2]。
3. 乳腺肿瘤中 HER2 低表达对患者预后的影响
目前,学术界对“HER2 低表达肿瘤能否作为独立预后因素”这一问题尚存争议[4]。从病理学缓解角度看,尽管多数研究结果显示新辅助化疗后 HER2 低表达乳腺癌患者的 pCR 低于 HER2-0 乳腺癌患者,但校正HR混杂因素后组间 pCR 差异并不显著[4]。另一项 Meta 分析结果与之相似——即在 HER2 低表达乳腺癌患者总体样本以及 HR+亚组中,观察到 HER2 低表达乳腺癌患者的 pCR 低于 HER2-0 乳腺癌患者,而在 HR-亚组中则未观察到显著差异[4]。从生存结局角度看,HER2 低表达肿瘤相比 HER2-0 肿瘤在研究结果上表现出“更优”、“更差”以及“无显著差异”并存的矛盾结果[4]。但即便如此也不可否认一些研究报道了 HER2 低表达肿瘤与 HER2-0 肿瘤之间存在预后差异[2]。尽管现有研究证据不支持 HER2 低表达作为独立的乳腺肿瘤表型,但仍为此类肿瘤提供了一个可用的治疗靶点[2]。
针对这一问题,欧洲肿瘤内科学会(ESMO)于 2023 年邀请来自 9 个国家的 32 位乳腺癌治疗领域带头专家召开多学科专家共识会议,其中,关于“HER-2 低表达是否为独特的分子亚型,与 HER2 0 表达肿瘤相比生物学特性是否不同”这一问题,ESMO 专家认为“HR 表达进行校正后,HER2 低表达与 HER2 0 表达肿瘤分子差异不显著。因此,HER-2 低表达不应被视为独特的分子亚型,而应被是为性质各不相同的一组肿瘤,其生物学特征主要取决于 HR 表达与否”。
三. HER2低表达乳腺癌的治疗
1. HER2 低表达乳腺癌治疗模式的发展与治疗现状
最初,研究人员尝试应用抗 HER2 单克隆抗体(mAb)治疗 HER2 低表达乳腺癌。其中与曲妥珠单抗相关研究(NSABP B 系列和 N9831)的最终结果显示其在 HER2 低表达乳腺癌中作用有限(见图 2)。而另一种 mAB——马吉妥昔单抗相关临床研究进展至 II 期时,即因疗效缺乏及不良反应而中断。此外,第一代抗体药物偶联物(ADC)恩美曲妥珠单抗(T-DM1)也曾被尝试应用于 HER2 低表达乳腺癌的治疗,但目前尚无相关正式临床试验[6]。
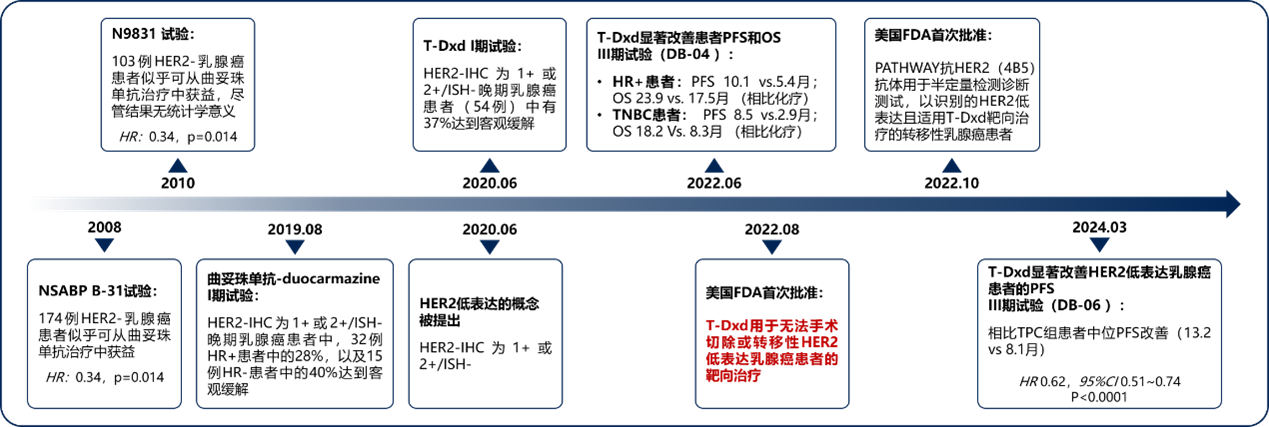
图片改编自:Current Biological, Pathological and Clinical Landscape of HER2-Low Breast Cancer. Fig 2.(结合文献7部分内容修改)
HER2:人表皮生长因子受体2;IHC:免疫组织化学染色法;ISH:原位杂交技术;PFS:无进展生存期;OS:总生存期;HR:风险比;CI:置信区间;HR:激素受体;TNBC:三阴性乳腺癌;T-Dxd:德曲妥珠单抗;TPC:紫杉醇+顺铂+卡培他滨化疗方案
图 2 HER2 低表达乳腺癌治疗模式的发展旅程[6,7]
二代 ADC 类药物德曲妥珠单抗(T-Dxd)是美国食品药品监督管理局(FDA)首个批准用于无法手术切除或转移性 HER2 低表达乳腺癌患者的靶向药物(见图 2)[6]。其关键临床 III 期 DB-04 的另一积极影响在于促使该研究中单克隆 IHC 抗体(PATHWAY 抗 HER2/4B5 兔单克隆抗体)检测系统的上市前批准,用于识别 HER2 低表达且适用 T-Dxd 靶向治疗的转移性乳腺癌患者(见图 2)[8]。
基于 DB-04 研究结果,国内外多个指南均增加 T-Dxd 作为 HER2 低表达患者推荐方案。如,中国临床肿瘤学会(CSCO)2024 年新版指南中对 HER2 低表达晚期乳腺癌患者的治疗给出系统性建议如下(见表 1)[9]:
表 1 CSCO 乳腺癌诊疗指南中关于 HER2 低表达乳腺癌的治疗建议[9]
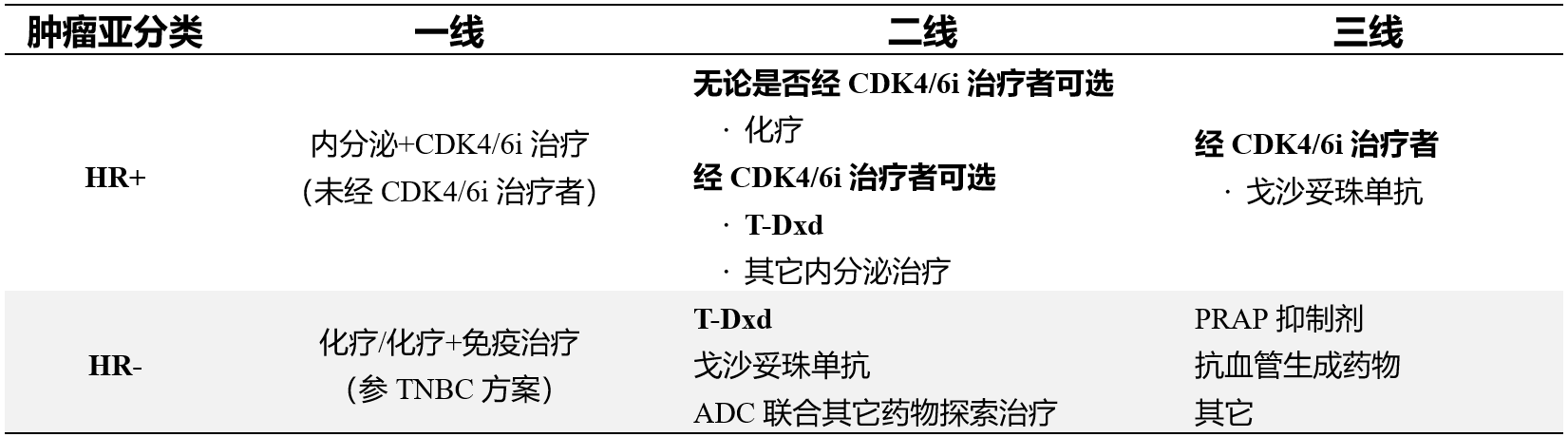
CDK4/6i:细胞周期蛋白依赖性激酶 4/6 抑制剂;T-Dxd:德曲妥珠单抗;TNBC:三阴性乳腺癌;ADC:抗体药物偶联物;PRAP:聚 ADP-核糖聚合酶
随着 DB-06 研究的结果发布,有望将 T-DXd 的治疗获益人群进一步拓展至 HER2 超低表达。目前,美国国立综合癌症网络(NCCN)指南在 2025 年最新版指南中微调了 T-Dxd 在 HER2 低表达乳腺癌中的用药建议——即 T-Dxd 可用于 HER2-IHC 评分为 0+、1+或2+/ISH-,且既往在肿瘤转移情况下接受过至少一种内分泌治疗的患者[10]。
2. 涉及HER2低表达乳腺癌治疗的药物机制及相关新药临床研发现状
已有多类药物涉及 HER2 低表达乳腺癌治疗,除前文 mAb 及 ADC 外,还包括双特异性抗体(bsAb)和疫苗类药物等,这些药物通过不同机制发挥抗肿瘤作用(见图 3)[1]。
1)mAb 类:此类药物包括多种可与 HER2 不同结构域结合的抗体,可通过抗体依赖性细胞毒性或抑制 HER2 异二聚化等机制发挥抗肿瘤活性。对 HER2 低表达乳腺癌患者,尽管前文提及相关药物(如曲妥珠单抗等)的作用有限,但临床前研究结果明确显示此类药物的抗肿瘤活性,进而推动其它此类新药后续的临床研发(见表 2)[1]。
2)ADC 类:ADC 是一种将 mAb 与抗肿瘤细胞毒性药物共价结合的偶联药物,其由载体(mAb)、有效载荷(细胞毒性药物)和连接子组成[1]。在机制方面,以前文提及的关键药物 T-Dxd 为例:在 HER2 低表达乳腺肿瘤中,T-Dxd 作用机制不太可能侧重 HER2 相关信号通路的阻断,而在于 HER2 低表达为 T-Dxd 结合提供了靶点。在两者结合后,T-Dxd 被肿瘤细胞内化,并受肿瘤溶酶体酶影响而裂解并分离有效载荷,后者可被递送至肿瘤细胞核中并诱导细胞死亡。此外,这些有效载荷具有膜渗透性,可以通过旁观者效应(通过渗透作用进入邻近肿瘤细胞)发挥抗肿瘤活性(见图 4)[2]。除 T-Dxd 外,尚有多种 ADC 类新药已在早期临床研究中显示出抗肿瘤活性,后续研究尚在进行中(见表 2)。
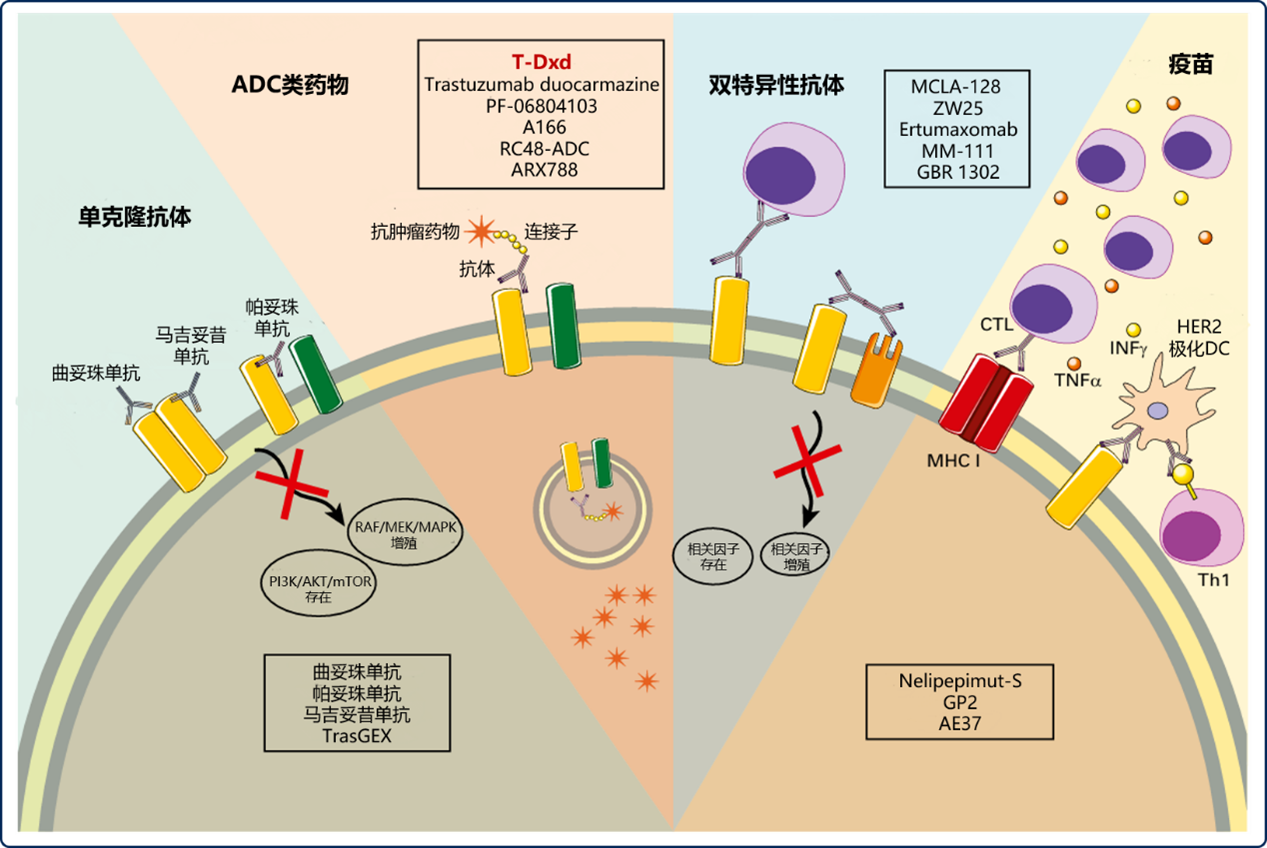
图片改编自:HER2-Low Breast Cancer: Pathological and Clinical Landscape. Fig 2.
PI3K:磷脂酰肌醇激酶;AKT:蛋白激酶 B;mTOR:哺乳动物雷帕霉素靶蛋白;RAF:即 MAPKKK,激活 MEK(MAPKK)的激酶;MEK:一种 MAPKK,即激活 MAPK 的激酶;MAPK:丝裂原活化蛋白激酶;CTL:细胞毒性 T 淋巴细胞;TNF-α:肿瘤坏死因子-α;INF-γ:干扰素-γ;HER2:人表皮生长因子受体 2;DC:树突状细胞;Th1:1 型辅助 T 细胞;MHC I:主要组织相容性复合体-I;T-Dxd:德曲妥珠单抗
图 3 涉及 HER2 低表达乳腺癌相关治疗药物的作用机制[1]
3)bsAb 类:bsAb 由靶向两个不同表位的 mAb 组成,其特点在于能够通过强制建立肿瘤-免疫细胞间的联系,以及向肿瘤微环境中递送有效载荷等多途径抑制肿瘤进展。目前已有数种抗 HER2 bsAb 在研,但只有少数研究纳入 HER2 低表达乳腺癌患者(见表 2)[1]。
表 2 各类涉及 HER2 低表达乳腺癌治疗新药相关临床研究
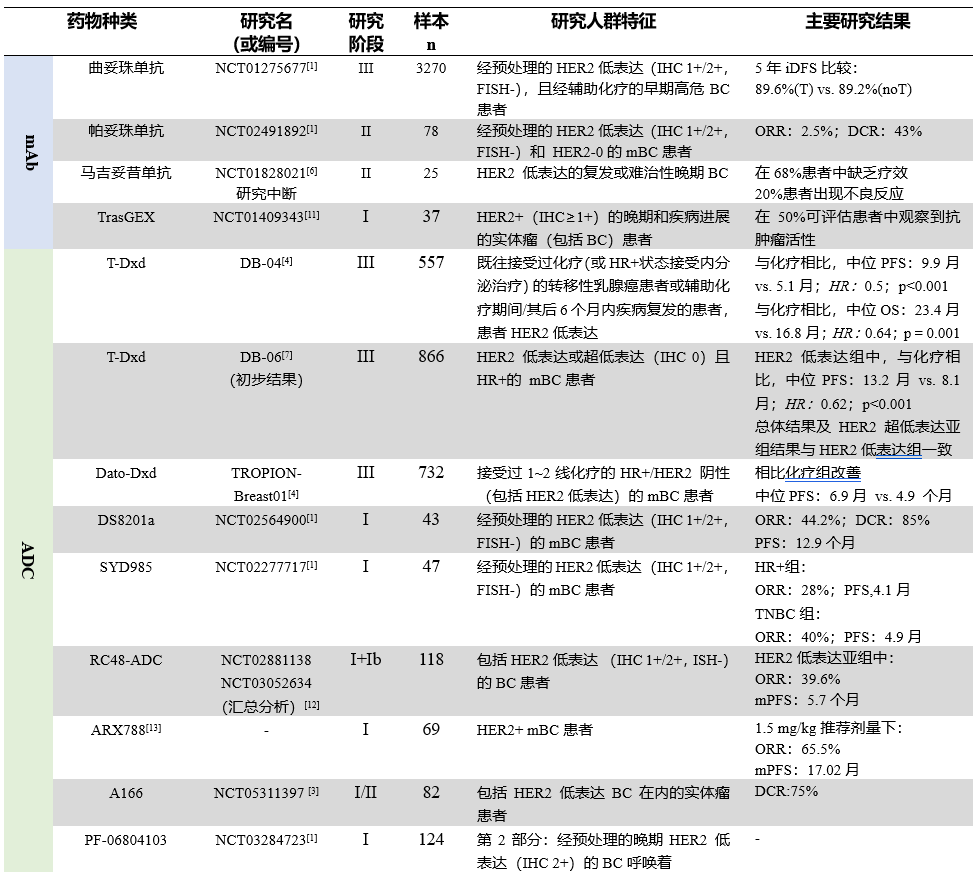
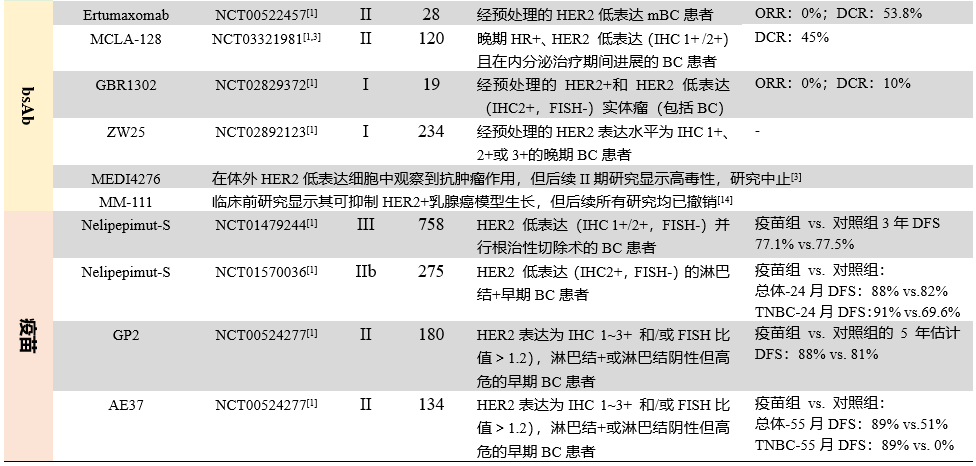
mAb:单克隆抗体;ADC:抗体药物偶联物;bsAb:双特异性抗体;HER2;人表皮生长因子受体 2;IHC:免疫组织化学染色法;FISH:荧光原位杂交技术;BC:乳腺癌;iDFS:无浸润性肿瘤复发生存率;T noT:使用或不适用曲妥珠单抗;HER2-0:IHC 评分为 0;ORR:客观缓解率;mBC:转移性乳腺癌;DCR:肿瘤经治疗后获得完全缓解(PR)+部分缓解(CR)+疾病稳定(SD),即肿瘤缩小没有达到 30%,但也没有达到进展的程度的患者比例;T-Dxd:德曲妥珠单抗;ISH:原位杂交技术;PFS:无进展生存期;OS:总生存期;HR+:激素受体阳性;HR:风险比;mPFS:中位无进展生存期;TNBC:三阴性乳腺癌
4)疫苗:接种恶性肿瘤相关疫苗,可增强针对肿瘤相关基因的免疫反应,以达到肿瘤防治目的。在乳腺癌领域,多数疫苗免疫疗法相关研究旨在改善患者早期结局。由于大多数乳腺肿瘤 HER2 高表达的特点,使得抗HER2疫苗逐步被研发,这些疫苗在 HER2+且低表达的乳腺癌中也开展了一些应用研究(见表 2)[1]。
四. HER2低表达乳腺癌诊疗中的争议与挑战
自“HER2 低表达”概念被提出至今,学术界对 HER2 表达——尤其在与肿瘤生物学相关方面的认识显著深入,但目前仍存在大量颇具争议性和挑战性的问题亟待解决[6]。这些问题涵盖了 HER2 低表达乳腺癌诊疗的方方面面,其重点可归纳为以下几点。 1)当前临床实践中HER2表达测量方法存在局限性,如何制定研发最合适且准确的“识别HER2低表达乳腺癌患者以及预测患者预后”的检测方法[4,6]?
HER2 检测手段在识别 HER2 低表达乳腺肿瘤方面存在差异——归因于实验室差异以及对监测结果的不同释义。就目前常用的 IHC 而言,尽管其简便易行且具有成本优势,但其半定量性质可能导致病理学家对观察结果的差异化。因此当 T-DXd 可用于治疗 HER2 低表达乳腺肿瘤后,医生需要新的“准确识别 HER2 低表达乳腺癌”相关指南建议[4]。
ASCO 和 CAP 最近更新了 HER2 乳腺癌相关指南,尽管更新后主要沿用 2018 年相关推荐[4],但新版指南也为病理学家在出具 IHC 报告时提供了若干建议[4](如使用标准化 IHC 评分,应用正确倍数显微倍镜,疑似结果重复检测等[8]),以助力筛查 HER2-乳腺癌患者中符合 T-Dxd 治疗条件的人群[4]。
应用定量 HER2 表达测量工具可能有助于克服此问题。定量连续评分(QCS)是一种基于深度学习的图像分析模型。值得注意的是,相关验证分析显示 QCS 可检测 HER2-乳腺癌中 HER2 表达的空间分布,并能将 T-DXd 治疗的 HER2 低表达人群分至高/低 QCS 两个亚组,且两个亚组患者的客观缓解率(ORR)和 PFS 不同。这些结果表明,HER2-QCS 可能有助于识别 HER2 低表达人群中 T-DXd 的潜在适应人群并预测其预后[4]。此外,有学者通过将常规组织病理检查与定量免疫荧光和质谱标准化 HER2 阵列相结合的方式,提出了检测 HER2 低表达肿瘤的新方法(HER2-V2),尽管该方法存在“高度依赖组织微阵列”的局限性,但也值得进一步研究[4]。
2)靶向 HER2 的 ADC 在 HER2-0 乳腺癌中的应用潜力如何?
除 HER2 低表达肿瘤外,相关研究也显示部分 HER2-0 乳腺癌患者可能从靶向 HER2 的 ADC 治疗中获益。如在 II 期 DAISY 试验中观察到有 HER2-0 乳腺癌患者在接受 T-Dxd 治疗后出现完全缓解。此后,该实验进一步分析了 HER2 表达水平与 HER2-0 乳腺癌患者对 T-Dxd 的关联。最终结果显示,无论 ERBB2(表达酪氨酸激酶受体 2 的基因)表达如何,T-Dxd 治疗对这部分患者均有潜在疗效。上述结果支持未来在 HER-0 乳腺癌患者中开展 ADC 相关临床试验[4]。
3)为达到最佳治疗结局,应如何规范选用ADC类药物并决定其序贯治疗顺序[4,6]?
过去的 20 年中 ADC 类药物在靶点多样性、有效载荷比和连接子设计方面经历了重大演变,药物疗效逐步提高,但在规范选用 ADC 类药物并决定其序贯治疗顺序这一问题上仍需进一步探索[4]。为达到最佳治疗结局,ADC 耐药和不良反应是医生必须考虑的问题。在耐药方面,靶点及有效载荷都可能是导致 ADC 耐药的原因,需要进行综合分析。而在不良反应方面,ADC 相关不良事件同样因药物靶点和有效载荷而异,因此最佳 ADC 治疗方案应综合考量患者个体因素及药物特征性不良反应[4]。想要解答上述问题,无疑还需要高质量的真实世界证据、前瞻性研究及大型转化分析结果支持[4,6]。
除上述问题外,HER2 低表达乳腺癌诊疗中还面临其它诸如表型定义优化、诊断质控、药物联合方案制定、安全性检验等问题[6]。未来仍需要多方研究以深入探索
总结
HER2 作为影响乳腺癌治疗决策的重要生物标志物,其表达分类对乳腺癌诊疗而言至关重要。HER2 低表达乳腺癌是临床上常见的患者类型,其在目前权威共识中被看作一组多样化的肿瘤。在治疗方面,随着第二代 ADC 类药物 T-Dxd 进入临床,HER2 低表达乳腺患者的治疗迈入新阶段,直至目前已有多种多类新药在研。如今 HER2 低表达乳腺癌诊疗中仍面临多项争议与挑战,囊括表型定义优化、检测方案优化、诊断质控、药物方案及联合方案制定并安全性检验等内容,未来仍需要多方研究以深入探索。
参考文献:
[1] Tarantino P, Hamilton E, Tolaney SM, et al. HER2-Low Breast Cancer: Pathological and Clinical Landscape. J Clin Oncol. 2020 Jun 10;38(17):1951-1962.
[2] Curigliano G, Dent R, Earle H, et al. Open questions, current challenges, and future perspectives in targeting human epidermal growth factor receptor 2-low breast cancer. ESMO Open. 2024 Apr;9(4):102989.
[3] Lai HZ, Han JR, Fu X, et al. Targeted Approaches to HER2-Low Breast Cancer: Current Practice and Future Directions. Cancers (Basel). 2022 Aug 3;14(15):3774.
[4] Kang S, Kim SB. HER2-Low Breast Cancer: Now and in the Future. Cancer Res Treat. 2024 Jul;56(3):700-720.
[5] Tarantino P, Viale G, Press MF, et al. ESMO expert consensus statements (ECS) on the definition, diagnosis, and management of HER2-low breast cancer. Ann Oncol. 2023 Aug;34(8):645-659.
[6] Zhang H, Peng Y. Current Biological, Pathological and Clinical Landscape of HER2-Low Breast Cancer. Cancers (Basel). 2022 Dec 25;15(1):126.
[7] Curigliano G, Hu X, Dent R A, et al. Trastuzumab deruxtecan (T-DXd) vs physician’s choice of chemotherapy (TPC) in patients (pts) with hormone receptor-positive (HR+), human epidermal growth factor receptor 2 (HER2)-low or HER2-ultralow metastatic breast cancer (mBC) with prior endocrine therapy (ET): Primary results from DESTINY-Breast06 (DB-06). Journal of Clinical Oncology, 2024, 42(17_suppl): LBA1000-LBA.
[8] Wolff AC, Somerfield MR, Dowsett M, et al. Human Epidermal Growth Factor Receptor 2 Testing in Breast Cancer: ASCO-College of American Pathologists Guideline Update. J Clin Oncol. 2023 Aug 1;41(22):3867-3872.
[9] 中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)乳腺癌诊疗指南2024 [Z]. 北京; 人民卫生出版社. 2024.
[10] NCCN. NCCN Clinical Practice Guidelines in Oncology:Breast Cancer(Version 2.2025)[EB/OL]. 2025[2025.03]. https://nccn.medlive.cn/guide/detail/837.
[11] Fiedler W, Stoeger H, Perotti A, et al. Phase I study of TrasGEX, a glyco-optimised anti-HER2 monoclonal antibody, in patients with HER2-positive solid tumours. ESMO Open. 2018 Jun 23;3(4):e000381.
[12] Wang J, Liu Y, Zhang Q, et al. RC48-ADC, a HER2-targeting antibody-drug conjugate, in patients with HER2-positive and HER2-low expressing advanced or metastatic breast cancer: A pooled analysis of two studies. J. Clin. Oncol. 2021;39:15.
[13] Zhang J, Ji D, Shen W, Xiao Q, Gu Y, O’Shaughnessy J, et al. Phase I trial of a novel anti-HER2 antibody-drug conjugate, ARX788, for the treatment of HER2-positive metastatic breast cancer. Clin Cancer Res. 2022;28:OF1–10.
[14] Gandullo-Sánchez L, Ocaña A, Pandiella A. HER3 in cancer: from the bench to the bedside. J Exp Clin Cancer Res. 2022 Oct 21;41(1):310.



