
前言
乳腺癌是最常见、死亡人数最多的女性恶性肿瘤,其中超2/3的晚期乳腺癌(ABC)患者是激素受体阳性 (HR+)、人表皮生长因子受体2阴性 (HER2-)。细胞周期蛋白依赖性激酶4/6抑制剂 (CDK4/6i)联合内分泌治疗是晚期/转移性乳腺癌治疗的基石。CDK4/6-视网膜母细胞瘤(RB)通路是细胞周期从G1期向S期转变的关键调控因子。CDK4/6i靶向CDK4/6酶复合物,阻滞细胞周期进程,防止细胞增殖失控。
目前被批准用于治疗HR+/HER2−晚期/转移性乳腺癌(ABC/MBC)的CDK4/6i包括哌柏西利、瑞波西利和阿贝西利。CDK4/6i关键研究证实,相比内分泌治疗+安慰剂,CDK4/6i联合内分泌治疗可改善绝经前/后患者的无进展生存期 (PFS)和总生存期 (OS)。基于此,CDK4/6i联合芳香酶抑制剂(AI)或氟维司群获批用于治疗乳腺癌。
真实世界证据对CDK4/6i的PFS、OS等疗效终点和毒副作用提供了重要洞见,同时允许对患者亚组进行分析,包括老年、体能较差或存在脑转移等通常被排除在RCT研究之外的患者。该研究旨在分析亚洲使用CDK4/6i治疗的HR+/HER2 - MBC患者的真实世界数据。
方法
患者和治疗
2015年至2020年,新加坡一项多中心队列研究纳入接受过CDK4/6i姑息治疗的ABC/MBC患者。回顾性数据收集时间为2015年1月1日至2020年7月31日,前瞻性数据收集时间为2020年8月1日至2020年12月31日。基于《赫尔辛基宣言》的规定,该研究得到了新加坡国家医疗保健组特定领域审查理事会 (NHG DSRB) (参考编号:2018/01081)和Parkway独立伦理委员会 (PIEC/2019/040)的批准。
该研究纳入来自新加坡三所国立学术卫生机构(新加坡国立大学癌症研究所、新加坡国家癌症中心和Tan Tock Seng医院)以及两个私人肿瘤组织(Icon癌症中心及癌症护理中心)的患者。从电子病历中提取患者的临床特征、肿瘤和治疗史,包括CDK4/6i适应症、停药时间和原因。内分泌治疗耐药定义为辅助内分泌治疗中或治疗结束12个月内疾病复发;内分泌治疗敏感定义为辅助内分泌治疗结束后>12个月疾病复发。出现下列情况时应停止治疗:疾病进展、不可耐受的毒性、患者死亡或患者决定停止治疗。
疗效
作为常规临床护理的一部分,临床医生每8-12周进行一次胸部和/或腹部CT扫描和/或骨骼扫描,以鉴定患者的治疗反应并对疾病进展进行评估。PFS定义为从开始用药到疾病进展或任何原因导致死亡的时间;OS定义为从起始给药到任何原因死亡的时间。安全性分析:检查临床医生记录的不良事件(AEs)发生率。剂量延迟 (DD)指28天(±2天)周期内出现的未按治疗计划使用CDK4/6i的次数;剂量减少 (DR):处方药物的剂量减少。将所有接受≥1个周期CDK4/6i治疗的患者纳入生存分析。
统计分析
采用Kaplan-Meier生存曲线对PFS和OS进行生存分析。单变量和多变量生存分析采用Cox比例风险回归模型。Cox回归的定量关联表示为风险比 (HR)与对应95%置信区间 (CI)。采用的所有统计检验均为双侧检验,p < 0.05被认为具有统计学意义。统计学分析采用IBM SPSS v22。
结果
患者基线特征、肿瘤及治疗特点
2015年1月至2020年12月,共有456例ABC/MBC患者接受CDK4/6i治疗。患者基线特征见表1。患者中位年龄59岁 (范围:24-92岁)。85名(19%)患者的年龄大于或等于70岁。大多数患者为华裔(n=326, 72%)、女性(n=454, 99%)、ECOG PS 为0/1 (n=356, 78%)和绝经后患者(n=344, 75%)。在绝经前患者 (n=107) 中,85例(79%)在内分泌治疗的同时接受卵巢功能抑制(手术或药物去势)。
表1 患者基线特征

大多数MBC为浸润性导管癌 (327例,72%)和ER阳性(448例,98%),17例(4%)患者为HER2+,半数患者为新发转移性MBC(226, 50%)。在228例(50%)疾病复发的患者中, 85例(37%)为内分泌治疗耐药、86例(38%)内分泌治疗敏感、27例(12%)患者未给予内分泌治疗。总共有17例(4%)患者为HER2+ BC;在起始CDK4/6i治疗时,25例(5%)为脑转移、31例(7%)为腹膜转移、145例(32%)为肝转移、244例(54%)为肺转移、342例(75%)为骨转移(表2)。
表2 患者的肿瘤和治疗特征
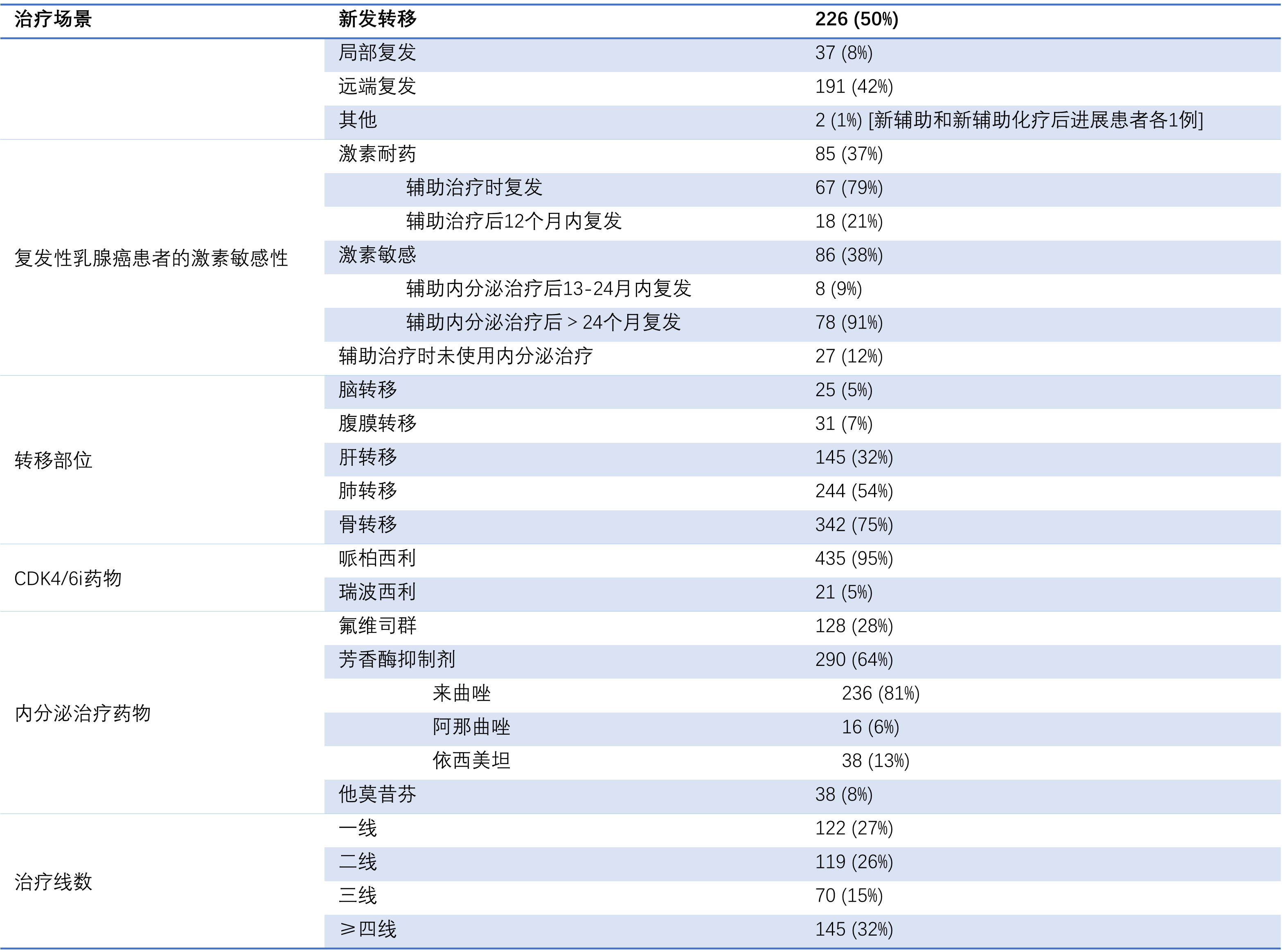
在该研究中,435例(95%)患者接受了CDK4/6i哌柏西利治疗。最常见的内分泌治疗联用药物为AI(n=290, 64%),其次是氟维司群(n=128, 28%)。其中,来曲唑是最常用的AI药物(n=236, 81%)。CDK4/6i最常用于晚期一线(n=122, 27%)和二线(n=119, 26%)治疗。图1显示2015-2020年期间CDK4/6i一线使用率逐年增加的趋势(图1)。
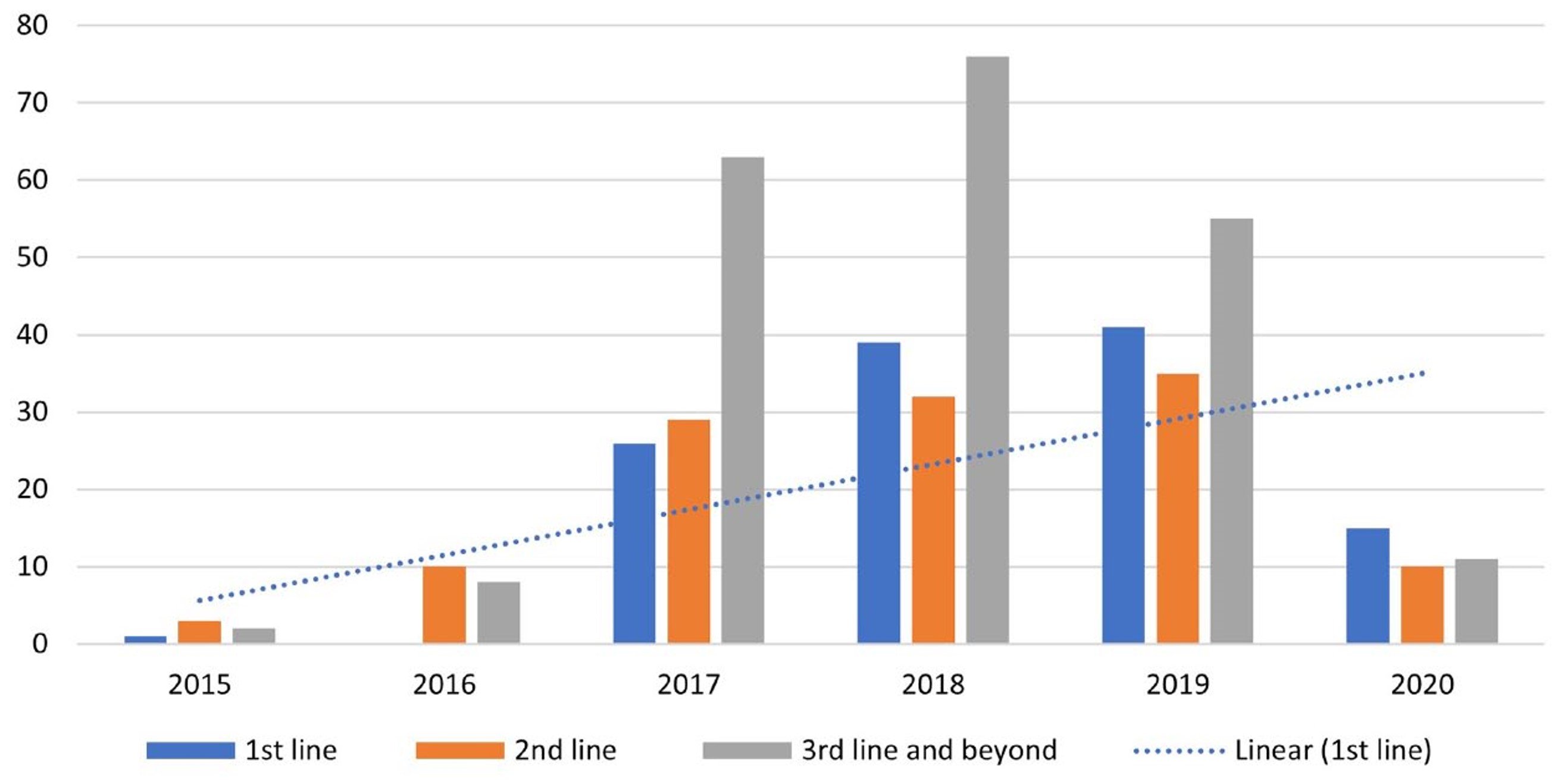
图1 2015-2020年期间CDK4/6i使用线数随时间变化的趋势
生存分析
所有患者均纳入生存分析。中位随访时间为30.1个月。一线、二线、三线和四线及以上治疗组患者的中位PFS分别为28.17、18.37、7.73和9.40个月[图2和图4(a)], 各亚组的24个月 OS率分别为72%、74%、56%、43% (图3)。
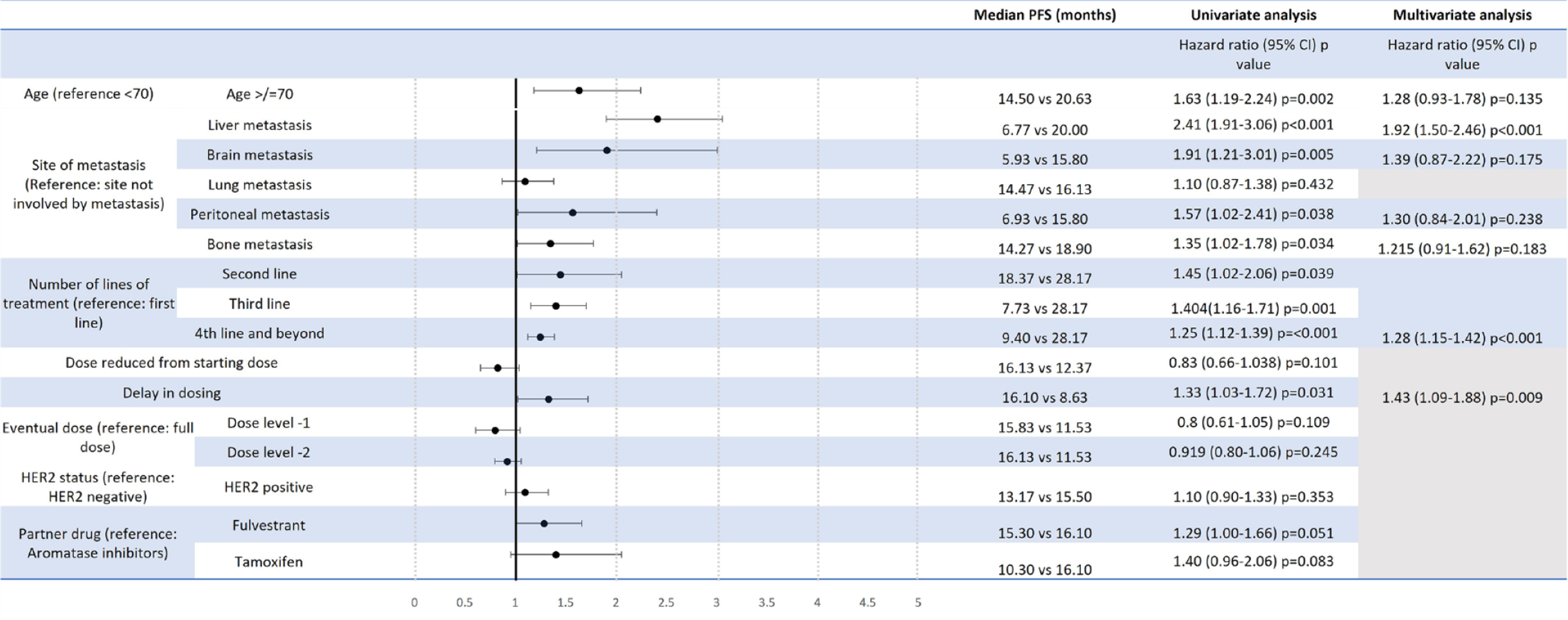
图2 PFS单因素与多因素Cox比例风险模型
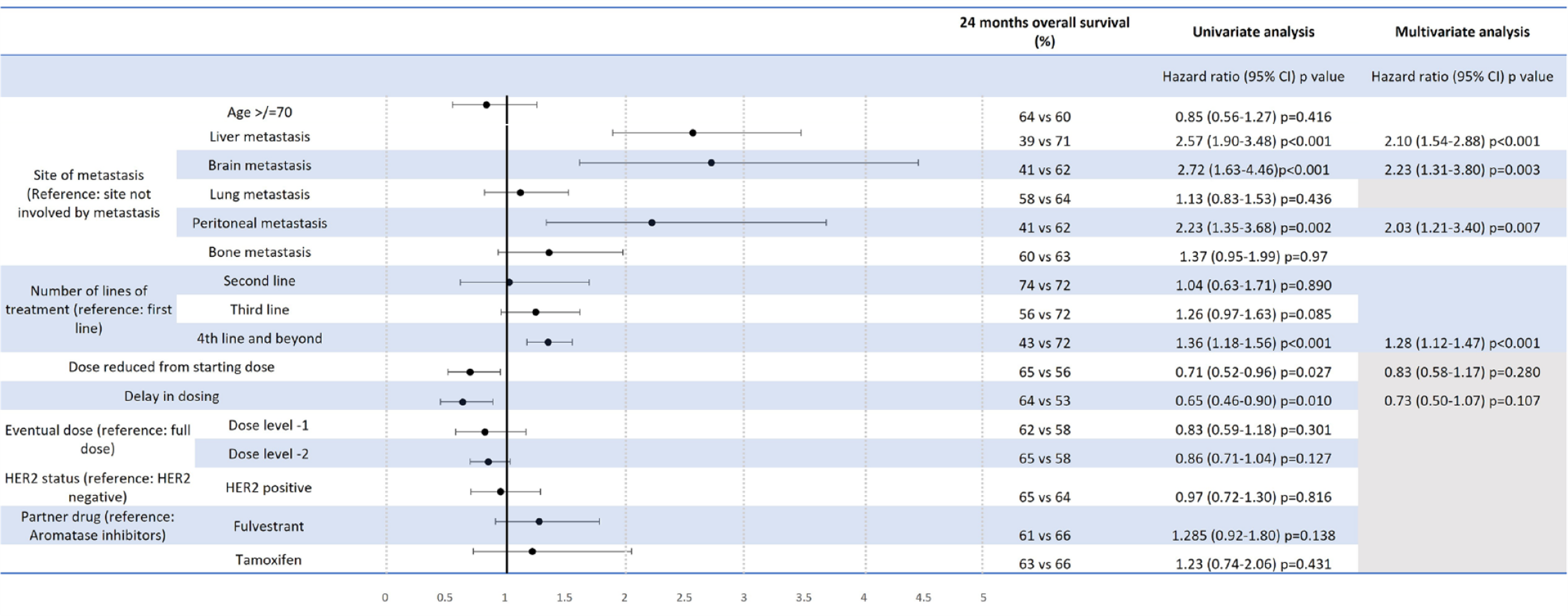
图3 OS单因素与多因素Cox比例风险模型
PFS和24个月OS率单变量分析结果显示,年龄≥70岁、基线存在肝、脑或腹膜转移以及使用CDK4/6i治疗的线数靠后与更短的PFS相关(图2)。肝转移 vs 无肝转移患者的PFS分别为6.77 vs 20.00个月 (HR=2.41, CI 1.91-3.06, p<0.001),年龄≥70 vs <70的患者PFS分别为14.50 vs 20.63个月 (HR=1.63, CI: 1.19-2.24, p=0.002) [图4(b)和(c)]。CDK4/6i低起始剂量与PFS缩短无关,标准剂量和低剂量起始CDK4/6i治疗的PFS分别为17.60和14.93个月(HR=1.01, CI: 0.75-1.35, P=0.960),见图4(d)。基线存在肝、脑或腹膜转移以及后线使用CDK4/6i治疗也与更短的OS相关(图3)。
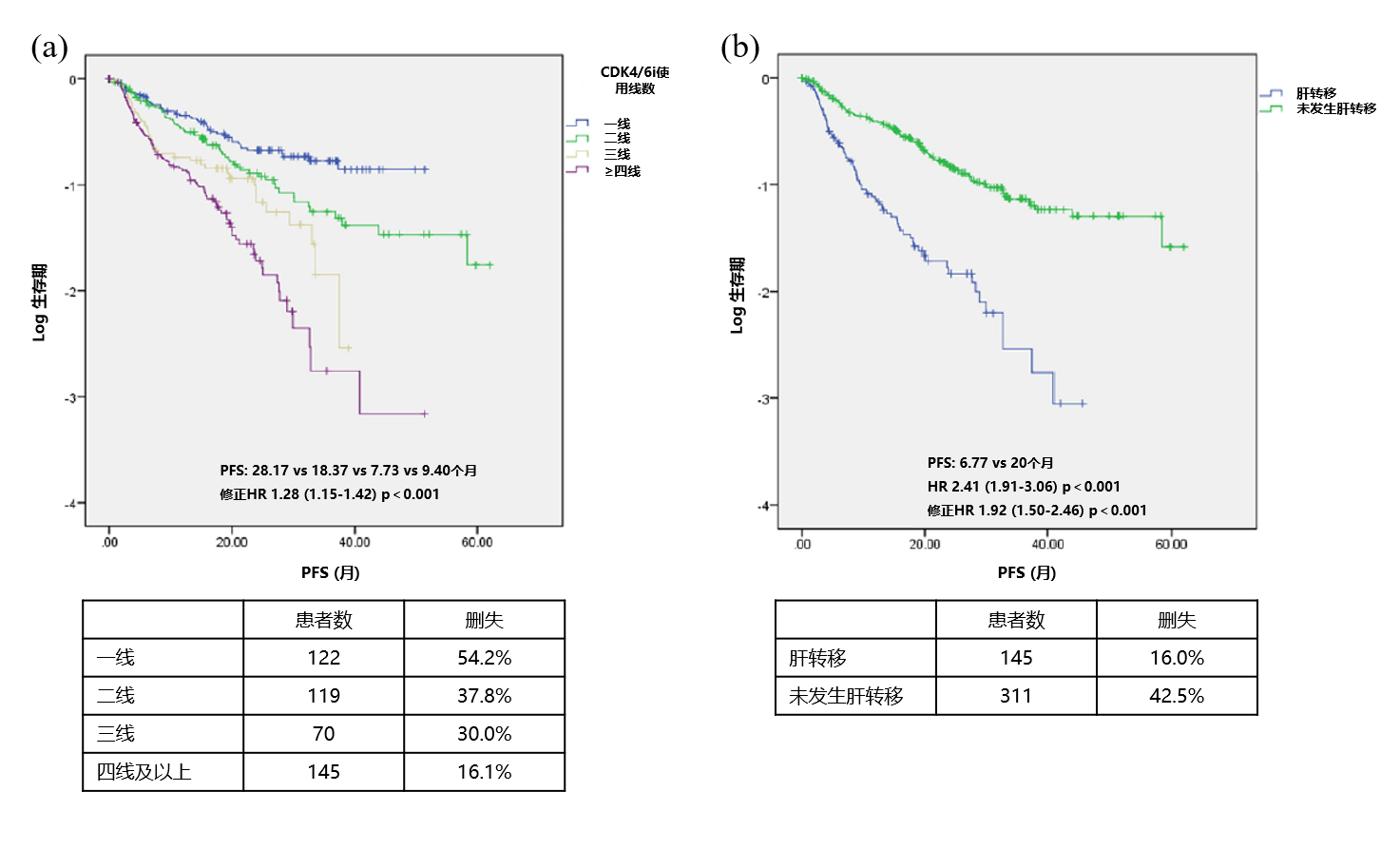
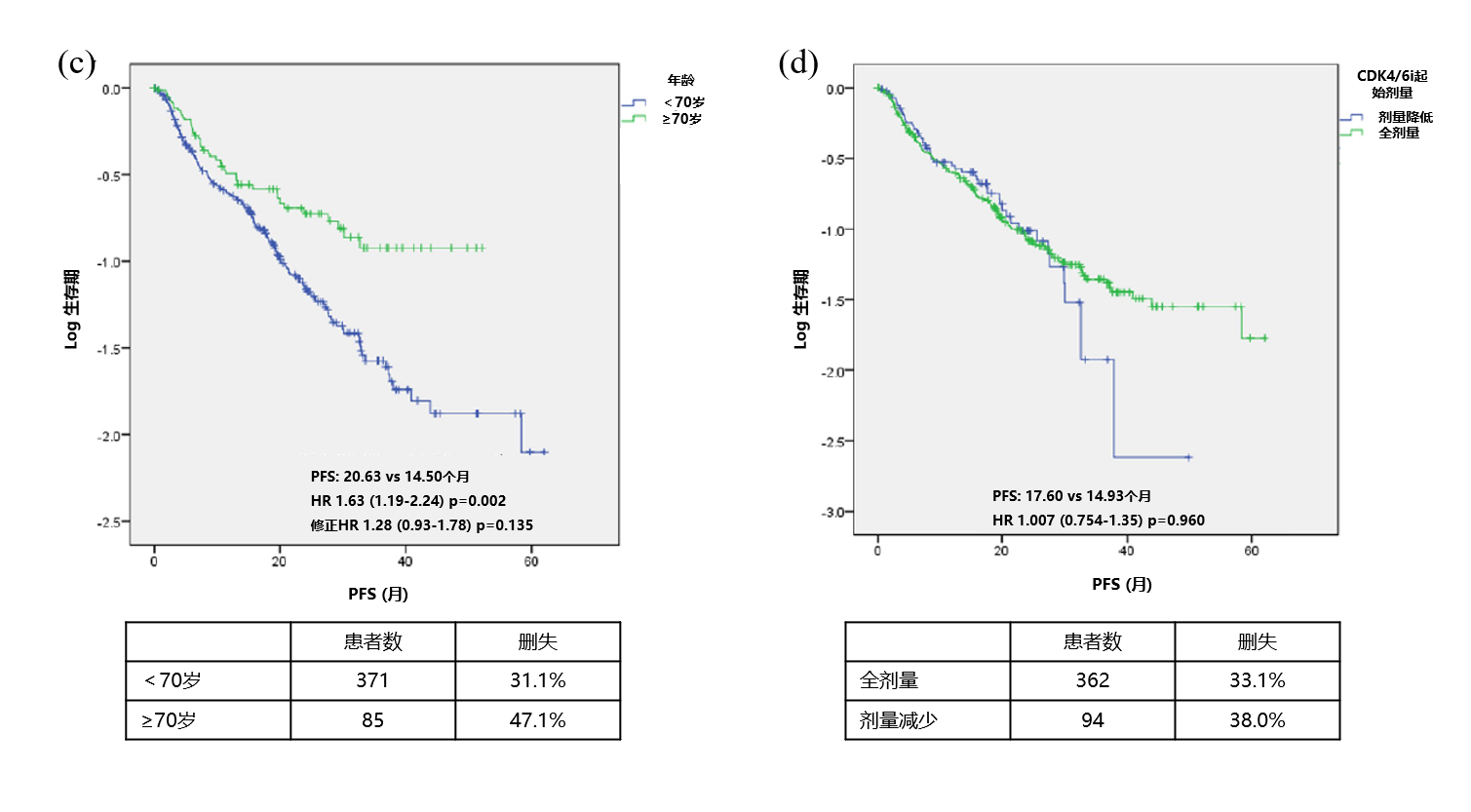
图4 PFS分层分析
a)使用CDK4/6抑制剂的治疗线数;b)存在肝转移;c)年龄;d) CDK4/6抑制剂起始剂量
PFS和OS多变量分析结果显示,基线肝转移和在后线使用CDK4/6i治疗仍与更短的PFS显著相关,而基线肝、脑、腹膜转移以及使用CDK4/6i治疗线数靠后仍与较短的OS显著相关(图2和3)。
剂量调整
共362名(80%)患者接受了FDA推荐的CDK4/6i起始剂量 (剂量水平1)。78名(17%)患者接受了较低的起始剂量:哌柏西利100mg或瑞波西利400mg (剂量水平-1),13名(3%)患者接受的起始剂量为哌柏西利75mg或瑞波西利200mg (剂量水平-2)[图5(a)]。年龄≥70岁和ECOG≥2与较低的CDK4/6i起始剂量显著相关(表3)。
表3 影响CDK4/6i起始剂量与最终剂量的因素

总体而言,217名(48%)患者至少需要一次DR, 88名(19%)患者有两次DR。在标准剂量起始治疗的患者中 (剂量水平1),195名(54%)患者至少需要一次DR。在101名(20%)低剂量起始治疗的患者中,22名(22%)患者需要进一步DR,11名(11%)患者最终剂量增加。大约三分之一的患者最终剂量分别为剂量水平1(37%)和剂量水平1(34%)。5例(1%)患者的最终剂量为哌柏西利125 mg/100 mg (n=2)、100 mg/75 mg (n=1)和75 mg[图5(b)]。仅年龄≥70岁与较低的最终剂量显著相关(表3)。
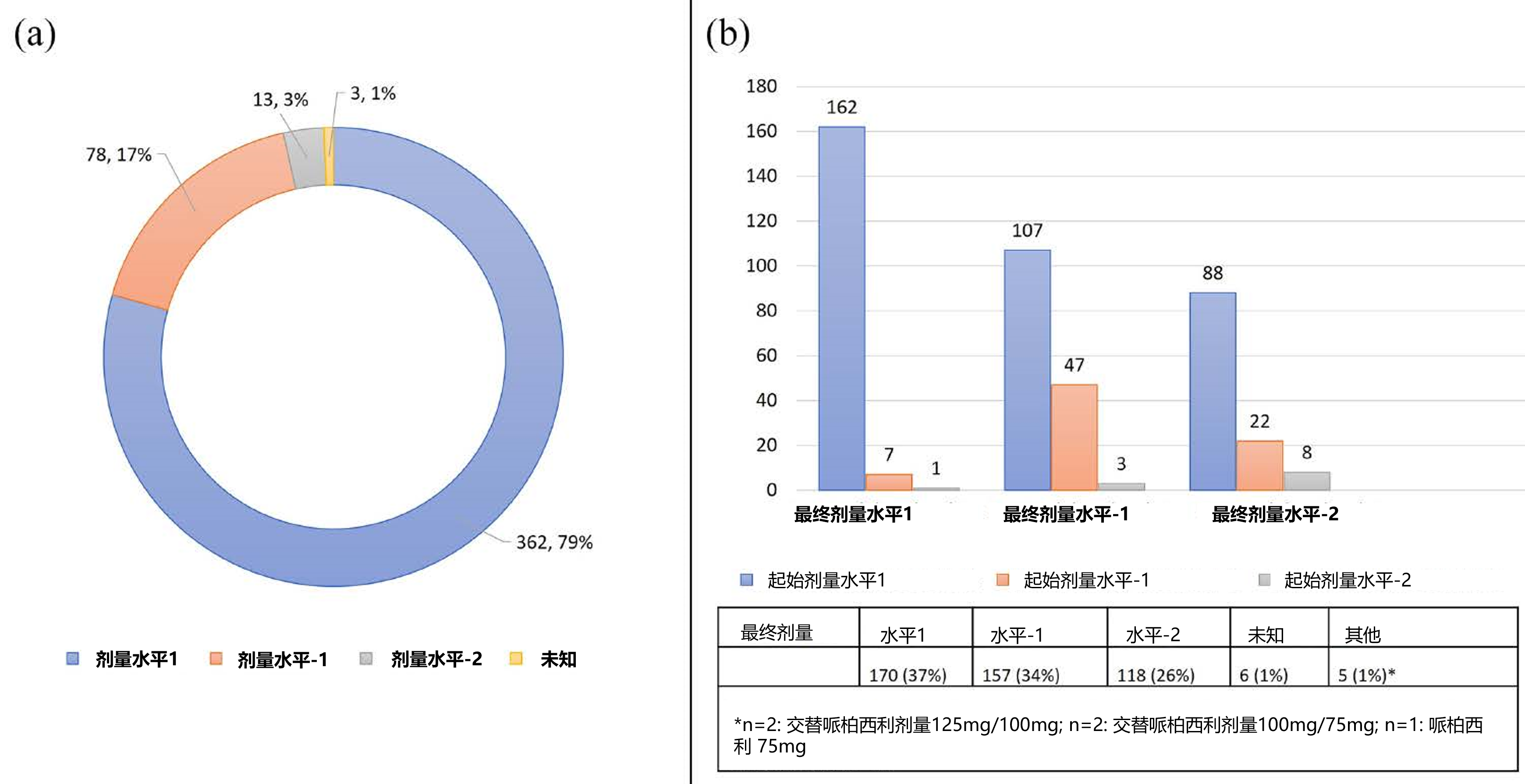
图5. CDK4/6抑制剂的起始剂量(a)和最终剂量(b)
总体而言,所有患者以及年龄≥70岁患者中分别有330(72%)名和63(74%)名患者至少发生一次DD。在该研究中,患者剂量延迟的总次数为1466次(每名患者的中位剂量延迟次数:2,范围:0-37)。部分患者因多种原因剂量延迟,最常见的原因是中性粒细胞减少症 (60%)。在剂量延迟事件中,有9例(2%)患者共计10起(0.7%)DD的发生与发热性中性粒细胞减少症相关(图6)。
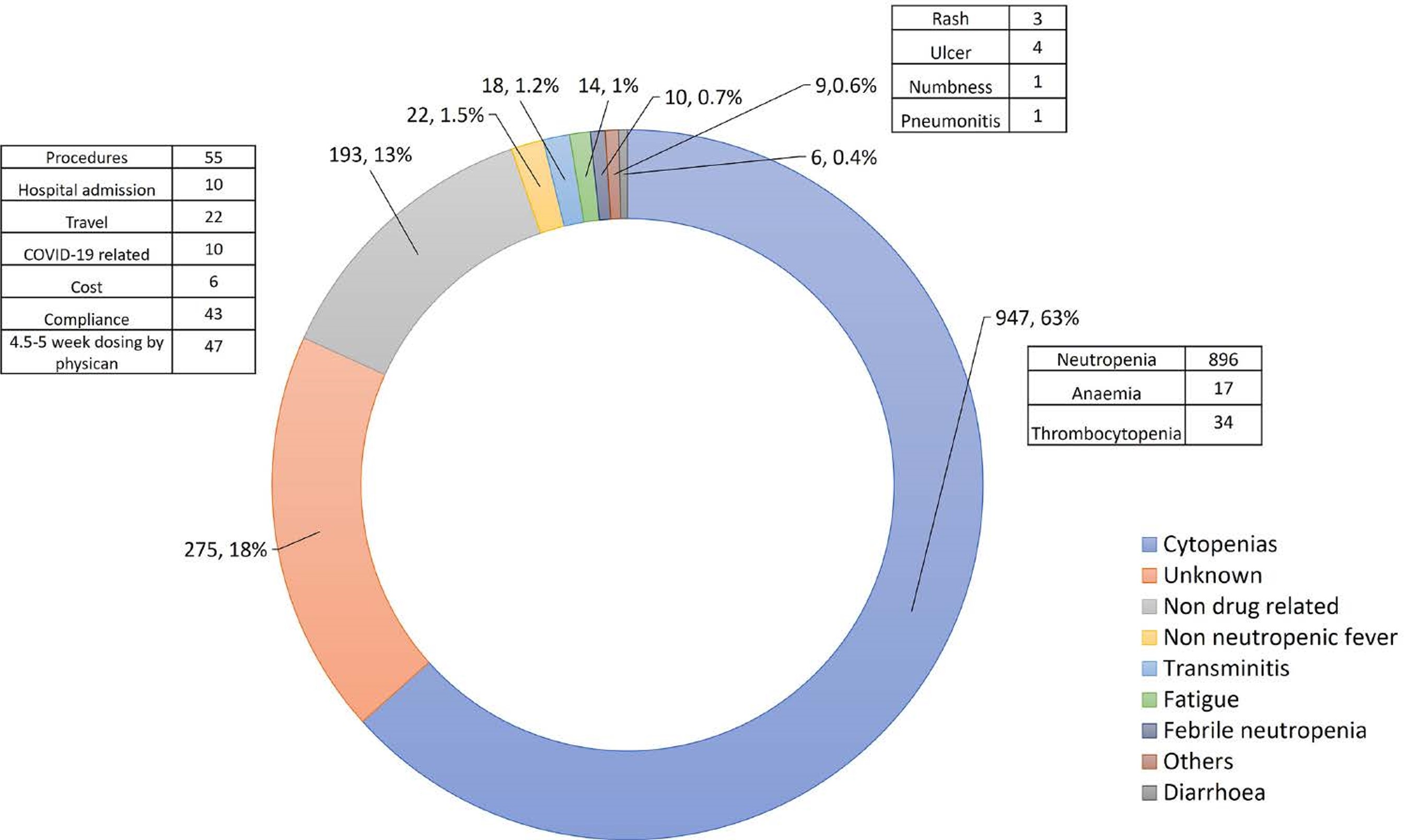
图6. CDK4/6抑制剂剂量延迟的原因
讨论
既往已有研究报道了真实世界中CDK4/6i的使用情况,其中最大的研究是来自Flatiron健康分析数据库的回顾性观察分析,该数据库包括1430名患者,其中1.6%是亚洲人。该研究是亚洲最大的真实世界研究,评估了CDK4/6i在ABC/MBC患者中的应用现状。结果表明,CDK4/6i是一种有效且安全的治疗方法,从2015年到2020年,CDK4/6i用于一线治疗的应用比例随时间呈增加趋势,疗效结果与临床试验结果一致。
与其他CDK4/6i真实世界研究相似,哌柏西利是该研究中患者最常使用的CDK4/6i。哌柏西利的广泛使用可能与哌柏西利是首个获批用于HR+/HER2- ABC/MBC治疗的CDK4/6i有关。与PALOMA-2(24.80个月)和MONALEESA-2研究(25.30个月)一线治疗结果相似,该研究中CDK4/6i一线治疗的中位PFS为28.17个月。该研究中报告的绝对PFS比Flatiron研究(20.00个月)和PALOMA-4研究(21.50个月)中哌柏西利联合来曲唑在亚洲绝经后妇女中的PFS更长。不同于PALOMA、MONALESSA和Flatiron研究,该研究中大多数患者是亚洲人(n=440, 97%)、以中国患者为主(n=326, 72%),再次验证了CDK4/6i在亚洲、特别是中国患者中的疗效。
尽管CDK4/6i已被FDA批准用于HR+/HER2- ABC/MBC患者的治疗,但老年或脑转移患者尚缺乏充足的循证证据。MONALEESA-2和PALOMA-2研究分别纳入295名(44%)和262名(39%)≥65岁的患者。尽管来曲唑+哌柏西利在≥65岁患者中显示出疗效获益,但≥70岁患者的比例以及此类患者是否从CDK4/6i+AI治疗中获益尚不明确。在该研究中,约20%的患者≥70岁,且单变量分析显示,≥70岁患者的PFS显著缩短。基线脑、肝或腹膜转移的患者PFS和24个月OS率也明显更短。
该研究中报道的CDK4/6i毒性与前瞻性临床试验中报道的毒性相似。最常见的AE是中性粒细胞减少症,仅2%的患者发生发热性中性粒细胞减少症。共217例(48%)患者需要至少一次DR,高于CDK4/6i II/ III期试验报告的35.5%-36.9%。这可能与该研究中更具异质性的患者构成相关,包括老年人和内脏转移患者。此外,CDK4/6i适应症申报研究纳入的患者大多是白人,而该研究主要纳入患者为亚洲人。不同种族患者的毒性特征存在差异。药物种族特异性可能解释了编码药物代谢酶的基因导致的抗癌药物毒性的种族间差异。值得庆幸的是,起始剂量减少、DR、DDs和CDK4/6i的最终剂量都与较差的PFS或24个月OS率无关。
该研究也存在一些局限性。该研究中的某些治疗组合或适应症与FDA批准的适应症不一致。例如,17例(4%)HER2+患者使用了CDK4/6i。尽管HER2+与HER2-患者在单变量分析中的PFS和24个月OS率均没有差异,但患者数量较少,无法得出明确结论。在该研究中,仅80%的患者使用CDK4/6i标准剂量起始治疗。此外,该研究的回顾性特点、不同的基线特征、接受不同CDK4/6i治疗患者数量的不平衡以及有限的样本量,都不允许在不同的CDK4/6i和亚洲人群中进行有效的疗效比较。
结论
该研究表明,CDK4/6i在真实世界中是一种有效且安全的治疗方法,与临床试验的结果一致。年龄≥70岁以及基线肝、腹膜或脑转移是不良预后因素。该研究观察到较多剂量调整,但剂量调整对生存没有影响。该结果向临床医生和患者证明了,当临床需要调整CDK4/6i剂量时,患者的生存结局不会受到负面影响。
参考文献
- Low JL, et al. Real-world outcomes from use of CDK4/6 inhibitors in the management of advanced/metastatic breast cancer in Asia. Ther Adv Med Oncol. 2022 Dec 18;14:17588359221139678. doi: 10.1177/17588359221139678.
文档编号:PP-PLB-CHN-0072



