
简要介绍
前列腺癌
1. J Clin Oncol:转移性前列腺癌的生殖系和体细胞基因组检测:美国临床肿瘤学会指南
2. Eur Urol:转移性去势抵抗性前列腺癌使用 PARP 抑制剂治疗效果的异质性:动态交互式系统综述与荟萃分析
3. Eur Urol:高危前列腺癌强化新辅助治疗后残余肿瘤负荷的长期结果和预后影响
4. Lancet Oncol:接受前列腺放疗患者急性与晚期毒性之间的相互关系:六项随机试验的个体患者数据荟萃分析
5. Eur Urol:3 期 IPATential150 试验中接受 ipatasertib(依帕他赛)和阿比特龙治疗患者的最终总生存期以及与临床结局相关的分子数据
肾癌
6. Eur Urol:更新的欧洲泌尿外科学会关于肾细胞癌的免疫检查点抑制剂辅助治疗及后续治疗的指南
7. Ann Oncol:III期随机 CLEAR 试验的生物标志物分析:仑伐替尼联合帕博利珠单抗对比舒尼替尼治疗晚期肾细胞癌
8. Lancet Oncol:消融治疗原发性局部肾细胞癌的比较疗效和安全性:一项系统回顾和荟萃分析
前列腺癌
1. 转移性前列腺癌的生殖系和体细胞基因组检测:美国临床肿瘤学会指南
发表期刊:J Clin Oncol
目的:评估转移性前列腺癌患者生殖系和体细胞基因组检测的相关证据,并给出推荐建议。
方法:由一个包含患者代表的多学科小组进行系统综述。检索 2018 年 1 月至 2024 年 5 月的PubMed数据库。若文章报道了接受生殖系或体细胞基因组检测的转移性前列腺癌患者情况,和/或对这些检测进行了比较,报道了检测率、预后信息或治疗意义,则入选。
结果:文献检索共识别出 1713 篇论文。应用纳入标准后,剩余 14 篇:8 篇系统综述和 6 项临床试验。
推荐意见:转移性前列腺癌患者应使用基于 panel 的检测方法同时进行生殖系和体细胞 DNA(脱氧核糖核酸)测序。这些检测能够指导多聚二磷酸腺苷核糖聚合酶抑制剂的使用,该抑制剂对转移性去势抵抗性前列腺癌患者具有生存获益。此外,生殖系检测可能对患者其他癌症的筛查具有意义,对家庭成员有级联检测意义。支持何时进行重复检测以及使用何种最佳组织类型(例如,原发性肿瘤、转移性活检与循环肿瘤 DNA[ctDNA] 检测)的数据较为有限,但本小组建议,对于先前检测结果为阴性或无信息价值的患者,考虑重新检测;当临床状态发生显著变化时,考虑进行转移性活检或 ctDNA 检测。仅与预后相关(而非预测)的二代基因组测序结果,不应在临床试验之外用于指导治疗。
2. 转移性去势抵抗性前列腺癌使用 PARP 抑制剂治疗效果的异质性:动态交互式系统综述与荟萃分析
发表期刊:Eur Urol
背景与目的:在转移性去势抵抗性前列腺癌(mCRPC)患者中,筛选出携带同源重组修复(HRR)基因突变且适合使用多聚二磷酸腺苷核糖聚合酶(PARP)抑制剂(PARPi)治疗的患者颇具挑战性。为了更深入地了解情况,我们对患有 mCRPC 且携带不同 HRR 基因突变的患者使用 PARPi 治疗的疗效差异进行了定量评估。
方法:本动态荟萃分析(LMA)采用动态交互式证据合成框架进行。我们纳入了评估 PARPi 作为单药治疗既往接受过治疗的 mCRPC 患者,或与雄激素受体通路抑制剂(ARPI)联合治疗初治患者的临床试验。针对按 HRR 状态、BRCA 状态及各基因分层的预设亚组进行随机效应荟萃分析。
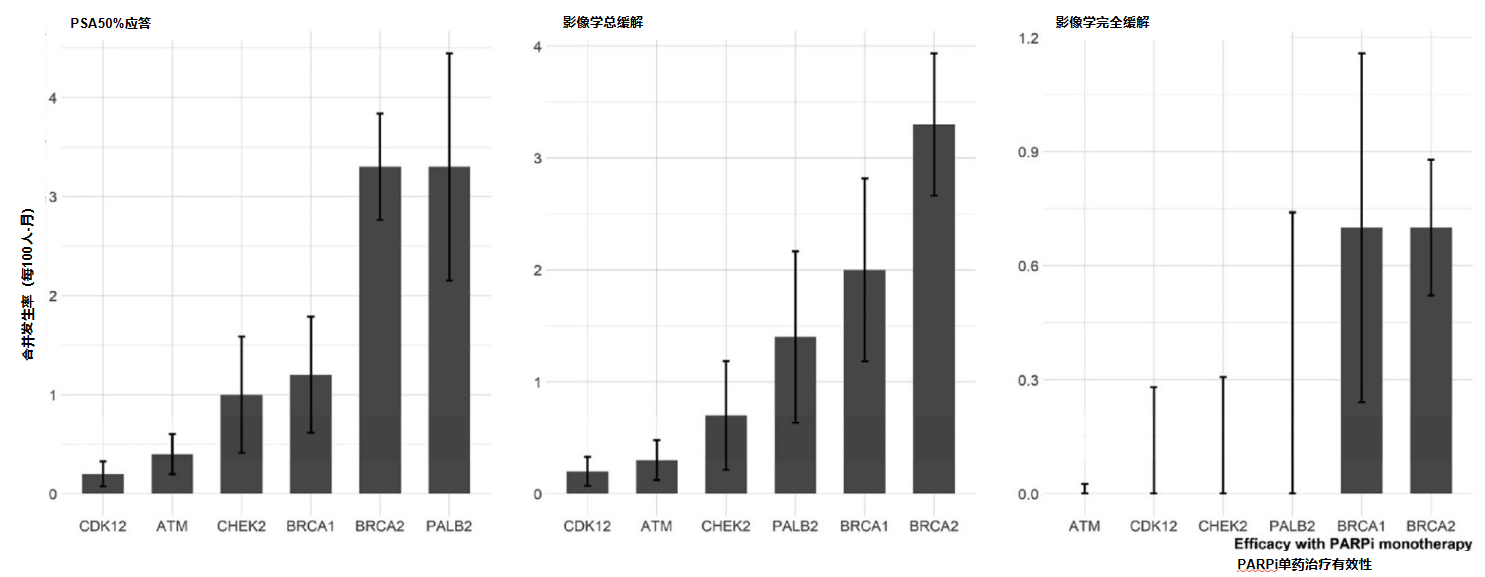
主要发现与局限性:本 LMA 的首份报告纳入了 13 项试验(共 4278 名患者)。如图 1 所示,在接受 PARPi 单药治疗的既往接受过治疗的 mCRPC 患者中,携带 BRCA2(前列腺特异性抗原应答率达 50%[PSA50%] 为 3.3;客观缓解率 [ORR] 为 3.3)、BRCA1(PSA50%为1.2;ORR为2.0)或PALB2(PSA50%为 3.3;ORR为 1.4)突变的患者每100人-月的肿瘤缓解率在数值上高于携带ATM(PSA50%为 0.4;ORR 为 0.3)、CDK12(PSA50%为 0.2;ORR 为 0.2)或 CHEK2(PSA50%为 1.0;ORR 为 0.7)突变的患者。在接受 PARPi+ARPI 联合治疗的患者中,携带 BRCA(HR=0.28,95%CI:0.13-0.62)或 CDK12(HR=0.58,95% CI:0.35-0.95)突变的患者,观察到有显著的影像学无进展生存期获益,但携带 PALB2(HR=0.53,95% CI:0.2 -1.32)、ATM(HR=0.93,95% CI:0.57 - 1.53)或 CHEK2(HR=0.92,95% CI:0.53-1.61)突变的患者则未观察到该获益。在对交叉治疗和后续治疗进行校正后,携带 BRCA 突变的患者观察到有总体生存获益(HR=0.47,95% CI:0.31-0.71),但携带 PALB2(HR=0.33,95% CI:0.10 - 1.16)、ATM(HR=0.97,95% CI:0.57-1.67)、CDK12(HR=0.80,95% CI:0.36-1.78)或 CHEK2(HR=0.81,95% CI:0.37-1.75)突变的患者未观察到该获益。
结论与临床意义:我们的 LMA 通过一个交互式网络平台,提供了关于 mCRPC 患者中 PARPi 治疗效果与特定基因突变相关性的信息。现有证据表明,携带 BRCA 突变的患者从 PARPi 治疗中获益最大,携带 PALB2 或 CDK12 突变的患者也有明显获益迹象,而携带 ATM 或 CHEK2 突变的患者则无获益。
图1.不同同源重组修复基因改变对 PARP 抑制剂(PARPi)单药治疗的疗效差异
3. 高危前列腺癌强化新辅助治疗后残余肿瘤负荷的长期结果和预后影响
发表期刊:Eur Urol
背景与目的:对于高危局限性前列腺癌(HRLPC),在根治性前列腺切除术(RP)前采用雄激素剥夺疗法(ADT)和雄激素受体通路抑制剂(ARPI)进行新辅助治疗(NAT),新辅助治疗后残余疾病程度的长期结果及其对预后的影响尚不清楚。
方法:我们分析了 2006 年至 2018 年间在我院五项评估 HRLPC 患者接受 6 个月 ARPI 新辅助治疗的试验中患者的数据。残余癌负荷(RCB)通过计算原发性肿瘤中根据细胞密度调整后的肿瘤体积来定量。主要结局是基于传统影像学检查的无转移生存期(MFS)。我们使用 Contal-O’Quigley 方法探索 RCB 分类,以区分 MFS 的高风险和低风险组。
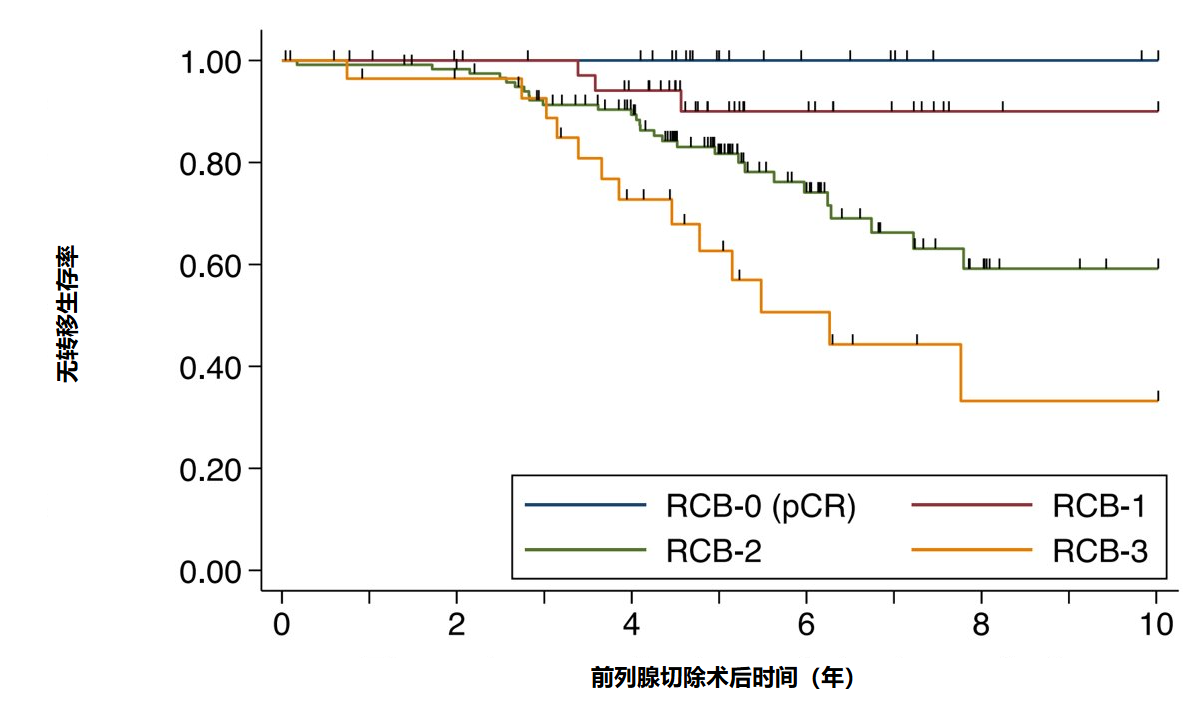
主要发现:在 218 例符合条件的患者中,诊断时前列腺特异性抗原中位数为 8 ng/ml,42 例(20%)患有 cT3-4 期疾病,154 例(71%)活检 Gleason 评分为 8-10 分。在 RP 时,24 例(11%)达到病理完全缓解,RCB 中位数为 0.05 cm³(四分位间距为 0.00-0.32)。中位随访 5 年,45 例患者发生转移,11 例死亡;5 年无转移生存率为 83%(95%CI:77-88%)。多变量分析显示,较高的 RCB 与较差的 MFS 相关(HR=1.21,95% CI:1.01 - 1.47)。如图 2 所示,RCB-0(病理完全缓解或无残余疾病)、RCB-1(<0.003 cm³)、RCB-2(0.003-0.672 cm³)和 RCB-3(>0.672 cm³)患者的 5 年无转移生存率分别为 100%、90%(95% CI:72-97%)、82%(95% CI:73-88%)和63%(95% CI:40-79%)。
结论与临床意义:HRLPC 患者在根治性前列腺切除术前接受 ARPI 新辅助治疗,其 5yr-MFS 为 83%。以 RCB 评估的病理缓解深度对 MFS 具有高度的预后预测价值。RCB 可用于指导 HRLPC 的新辅助治疗及新辅助治疗后的辅助治疗试验。
图2.根据残余癌症负担(RCB)类别分层的无转移生存的 Kaplan-Meier 曲线
4. 接受前列腺放疗患者急性与晚期毒性之间的相互关系:六项随机试验的个体患者数据荟萃分析
发表期刊:Lancet Oncol
背景:利用多项随机临床试验及不同分割放疗方案的数据,对前列腺放疗后急性毒性与晚期毒性之间关联的研究尚不充分。我们旨在描述接受常规分割或中度低分割前列腺放疗患者的急性和晚期泌尿生殖系统及胃肠道毒性之间的关系。
方法:这是一项个体患者数据荟萃分析,从前列腺癌随机试验荟萃分析(MARCAP)联盟中,识别出常规分割或中度低分割前列腺放疗的随机 3 期试验,这些试验需具备个体层面的急性和晚期毒性数据,且数据在 2023 年 12 月 1 日前可得。无个体患者数据的试验被排除。数据由研究人员向 MARCAP 提供。使用校正后的广义线性混合模型(校正年龄、雄激素剥夺治疗状态、放疗类型、辐射剂量和放疗方案),评估 2 级及以上急性(放疗后≤3 个月)和晚期(放疗后>3 个月)的泌尿生殖系统及胃肠道毒性之间的关系。在收集了扩展前列腺癌指数综合生活质量(QOL)评估的试验子集中,还评估了急性泌尿生殖系统和胃肠道毒性与泌尿和肠道生活质量至少两倍最小临床重要差异(MCID)的下降之间的关联。
结果:26 项可用试验中有 6 项符合所有纳入标准。共纳入 6593 例患者(常规分割:n=4248;中度低分割:n=2345)。中位随访时间为 72 个月(IQR 61-94)。2 级及以上急性泌尿生殖系统毒性,与 2 级及以上晚期的泌尿生殖系统毒性(优势比 2.20[95% CI 1.88-2.57],p<0.0001)以及至少两倍于 MCID 的泌尿生活质量下降(1.41[1.17-1.68],p=0.0002)相关。2 级及以上急性胃肠道毒性,与 2 级及以上晚期胃肠道毒性(2.53[2.07-3.08],p<0.0001)以及至少两倍于 MCID 的肠道生活质量下降(1.52[1.26-1.83],p<0.0001)相关。
结论:前列腺放疗后的急性毒性在统计学上与晚期毒性以及患者报告的生活质量指标下降显著相关。这些数据支持评估降低急性毒性的干预措施是否最终能降低晚期毒性风险的研究。
5. 3期 IPATential150 试验中接受 ipatasertib 和阿比特龙治疗患者的最终总生存期以及与临床结局相关的分子数据
发表期刊:Eur Urol
背景与目的:在 3 期 IPATential150 试验中,对于免疫组化(IHC)检测显示 PTEN 缺失的转移性去势抵抗性前列腺癌(mCRPC)男性患者,在阿比特龙基础上加用 ipatasertib 显著降低了疾病进展风险,但在意向性治疗(ITT)人群中未观察到此效果。在此,我们报告最终总生存期(OS)分析结果,并展示预先设定及探索性生物标志物分析的结果。
方法:患者被随机分配接受 ipatasertib(400毫克,每日一次)或安慰剂。所有患者均接受阿比特龙(1000 毫克,每日一次)和泼尼松(5 毫克,每日两次)治疗。对 IHC 检测显示 PTEN 缺失的患者及 ITT 人群进行总生存期评估。探索性生物标志物分析包括通过下一代测序(NGS)检测 PTEN 状态以及其他关键基因组改变。
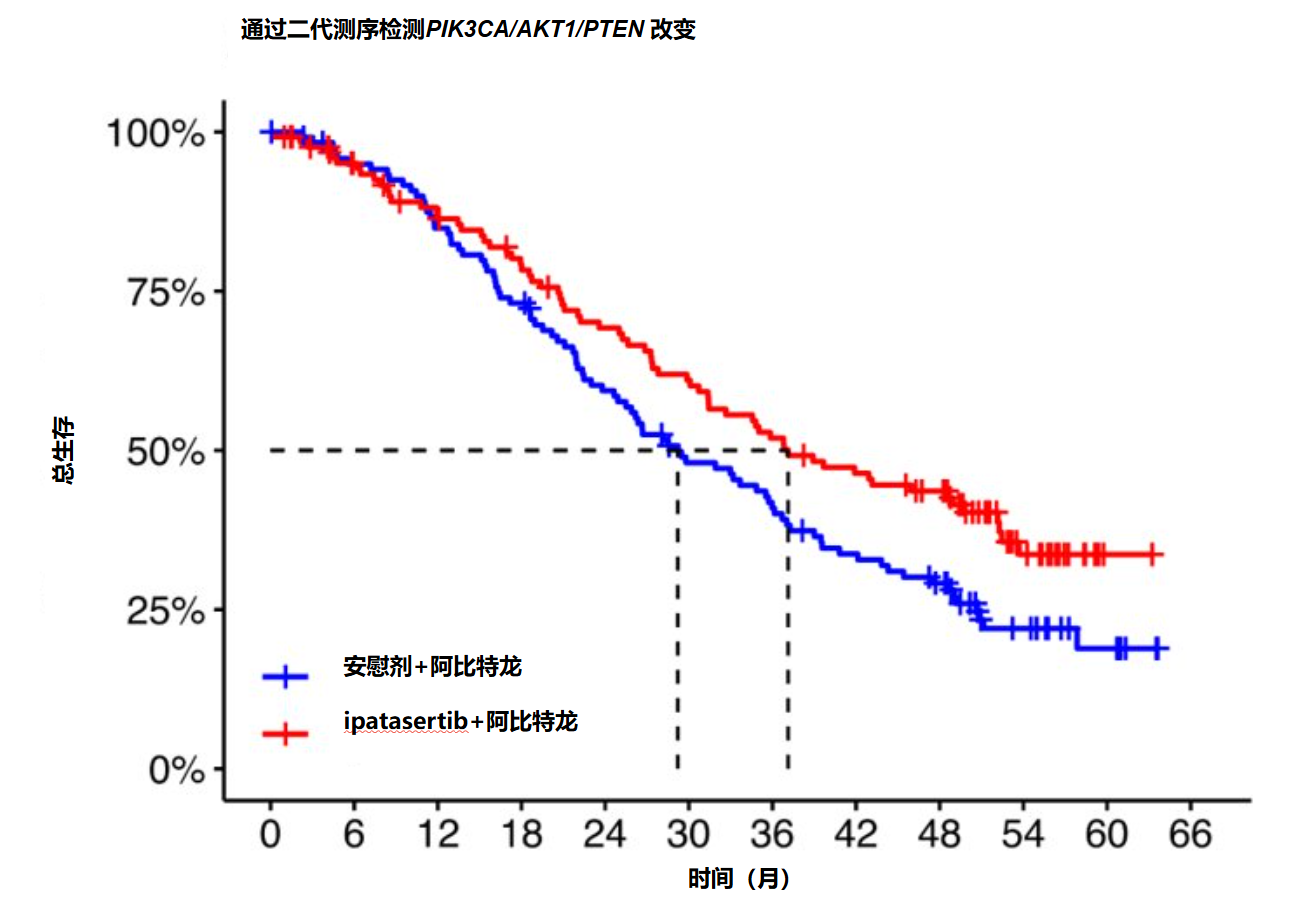
主要发现与局限性:在最终分析时(中位随访 33.9 个月),对于 IHC 检测显示 PTEN 缺失的患者(n=521;分层风险比[sHR]为 0.94,95%置信区间[CI]为 0.76-1.17;p=0.57)或 ITT 人群(n=1101;sHR为 0.91,95% CI 为 0.79-1.07;未进行正式检验),加用 ipatasertib 均未改善总生存期。探索性 NGS 评估确定了基因组 PTEN 缺失亚组(n=208,见图 3)或 PIK3CA/AKT1/PTEN 改变亚组(n=250见图 4),加用 ipatasertib 可能使这些亚组患者获得更好的结局(风险比分别为 0.76,95% CI 为 0.54-1.07;和 0.70,95% CI 为 0.51-0.96)。局限性包括分析具有探索性、NGS数据不完全可得以及患者体内可能存在异质性。
结论与临床意义:无论 IHC 检测的 PTEN 状态如何,对于 mCRPC 男性患者,在阿比特龙基础上加用 ipatasertib 均未改善总生存期。探索性生物标志物分析确定了其他基因组改变对 AKT 阻断剂在 mCRPC 中应用的潜在临床指导意义,这些需要在前瞻性研究中进一步验证。
图3.PTEN 缺失患者经 ipatasertib +阿比特龙与安慰剂+阿比特龙治疗后总生存的 Kaplan-Meier 曲线
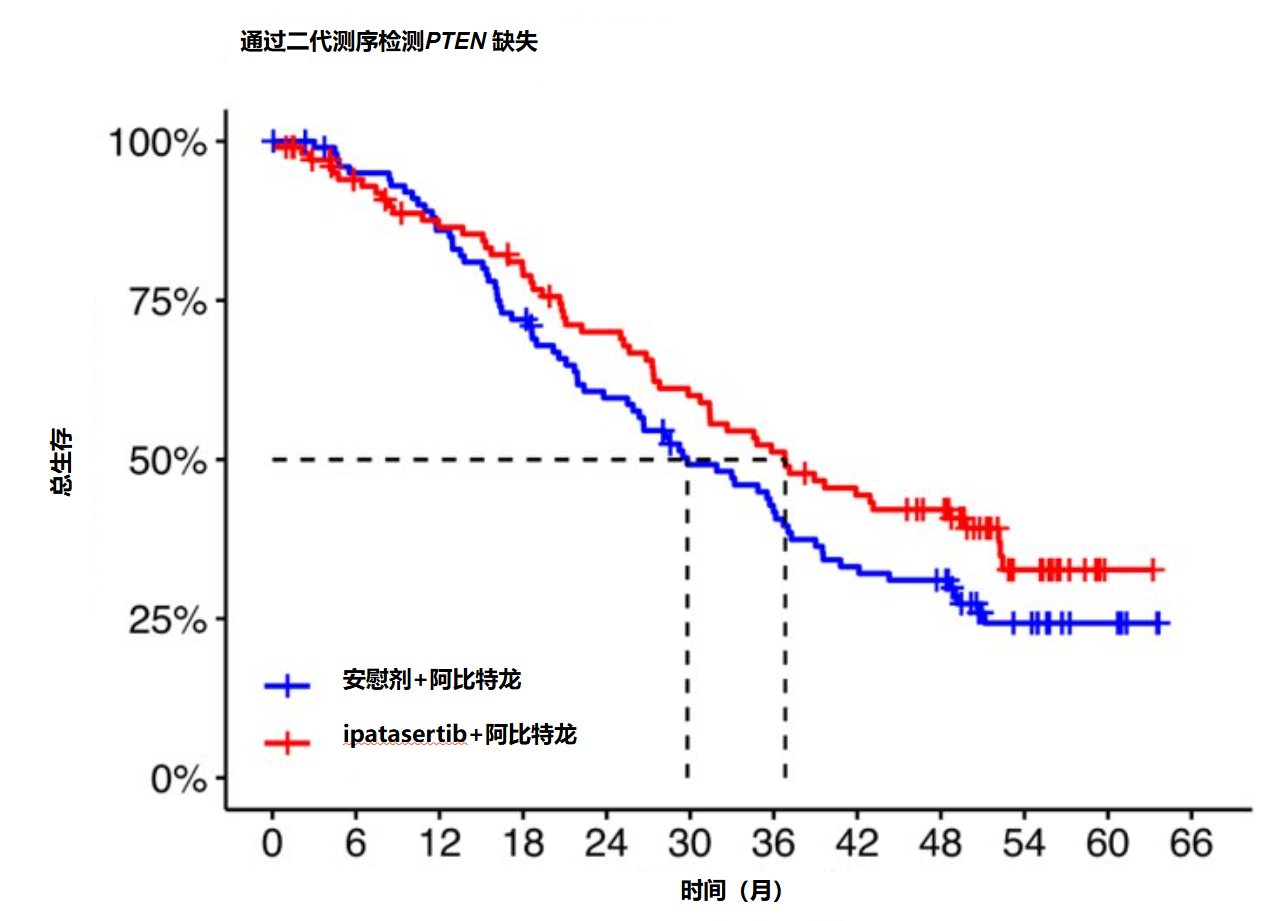
图4.PIK3CA/AKT1/PTEN 改变患者经 ipatasertib +阿比特龙与安慰剂+阿比特龙治疗后总生存的Kaplan-Meier 曲线
肾癌
6.更新的欧洲泌尿外科学会关于肾细胞癌的免疫检查点抑制剂辅助治疗及后续治疗的指南
发表期刊:Eur Urol
KEYNOTE - 564 试验表明,使用 PD - 1 抗体帕博利珠单抗进行辅助免疫检查点抑制剂(ICI)治疗,可显著提高具有高复发风险的局限性透明细胞肾细胞癌(RCC)患者的无病生存期(DFS)和总生存期(OS)。TiNivo 和 CONTACT - 03 试验报告了转移性肾癌患者在 ICI 治疗进展后接受后续治疗的结果。欧洲泌尿外科学会(EAU)肾细胞癌指南小组重新评估了这些新的试验结果,以更新关于辅助治疗和辅助治疗后治疗的建议。辅助使用帕博利珠单抗显著改善了总生存期(风险比 0.62,95%置信区间0.44-0.87;p=0.005)。近期关于转移性肾癌患者在 ICI 治疗复发后再次使用 ICI 的试验,并不支持在接受辅助ICI治疗期间或之后复发的患者中使用 ICI 单药治疗或联合治疗。目前尚无关于辅助使用帕博利珠单抗失败后治疗方案的前瞻性试验结果。基于近期研究结果,EAU 肾细胞癌指南小组更新了辅助治疗的建议,现在强烈推荐辅助使用帕博利珠单抗。不建议在辅助使用帕博利珠单抗期间或之后不久复发的患者中使用 ICI 单药治疗或联合治疗。
患者总结:中高危肾癌患者术后使用名为帕博利珠单抗的免疫治疗药物,可延缓癌症复发时间并延长生存期。因此,强烈推荐这些患者术后使用帕博利珠单抗。然而,相当一部分患者会出现影响生活或严重的副作用。
7. III 期随机 CLEAR 试验的生物标志物分析:仑伐替尼联合帕博利珠单抗对比舒尼替尼治疗晚期肾细胞癌
发表期刊:Ann Oncol
背景:在 CLEAR 试验中,与舒尼替尼相比,仑伐替尼联合帕博利珠单抗(L+P)在晚期肾细胞癌(aRCC)患者的一线治疗中显著提高了疗效。我们在此报告CLEAR试验生物标志物分析的结果。
患者与方法:对存档的肿瘤标本进行程序性死亡配体1(PD-L1)免疫组织化学(IHC)检测以及下一代测序分析(全外显子测序/RNA 测序)。对于基于 IHC 或 RNA 测序的分析,通过卡氏功能状态(KPS)评分进行校正后开展连续分析,具体包括:PD-L1 联合阳性分数(CPS)与最佳总体缓解(BOR)/无进展生存期(PFS)的关系;各基因特征评分[T 细胞炎性基因表达谱(TcellinfGEP)/非 TcellinfGEP 特征,包括增殖和血管生成相关特征]与 BOR/PFS 的关系。针对每组至少有 20 名患者发生致癌性改变的基因,分析肾细胞癌驱动基因的突变状态与 PFS 之间的关联。经基线 KPS 校正后,评估分子亚型与预后的关系。预先设定了所评估的生物标志物集以及 PD-L1 CPS、基因特征评分和分子亚型的统计学显著性标准。
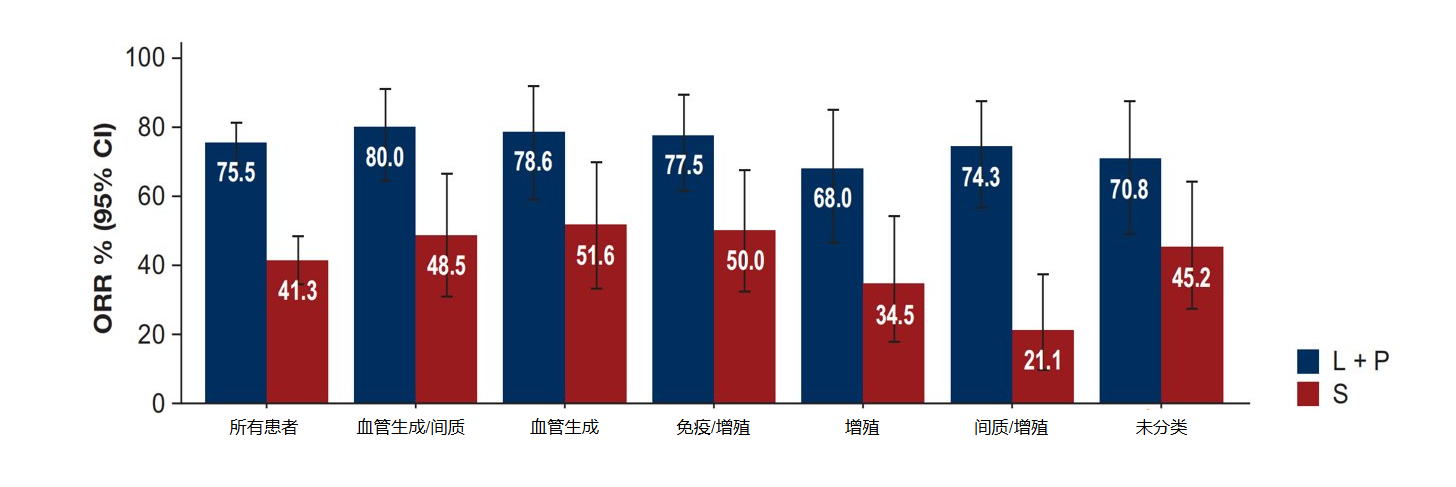
结果:采用连续值进行组内分析显示,两种治疗方案中,PD-L1 水平与 BOR/PFS 均无关联。无论肾细胞癌驱动基因(VHL、PBRM1、SETD2、BAP1、KDM5C)的突变或野生型亚组如何,两组之间的 PFS 风险比相似。对于 L+P 方案,未观察到 PFS 与基因特征评分之间存在关联。使用舒尼替尼治疗时,高增殖和 MYC 特征评分与较短的 PFS 相关;高血管生成和微血管密度特征评分与较长的 PFS 相关。定义了六种新的分子亚型。中低危患者的肿瘤在血管生成和血管生成/间质簇中富集;高危患者的肿瘤在增殖和未分类(低 TcellinfGEP/低血管生成/低增殖)簇中富集。在对 KPS 和与 PFS 分别相关的基因特征进行校正后,未观察到 L+P/舒尼替尼治疗的分子亚型与 PFS 之间存在相关性。
结论:在一系列用肾细胞癌驱动基因突变、PD-L1、基因表达特征和分子亚型定义的生物标志物亚组中,均观察到与舒尼替尼相比,L+P 方案在 aRCC 患者中的客观缓解率和 PFS 有所改善。
图5.各分子亚型患者接受仑伐替尼联合帕博利珠单抗(L+P)或舒尼替尼(S)相比治疗的 ORR
8. 消融治疗原发性局部肾细胞癌的比较疗效和安全性:一项系统回顾和荟萃分析
发表期刊:Lancet Oncol
背景:非侵入性和微创消融治疗,包括立体定向体部放疗(SBRT)、射频消融、微波消融和冷冻消融,已成为肾细胞癌的关键治疗选择,尤其适用于不适合手术的患者。我们旨在比较这些新兴治疗方法在局限性肾细胞癌患者中的临床疗效与安全性。
方法:在这项系统评价与荟萃分析中,我们检索了 PubMed(MEDLINE)、Embase 和 Cochrane 图书馆在 2000 年 1 月 1 日至 2024 年 3 月 1 日期间发表的文献。符合条件的文章包括观察性研究和随机对照试验,这些研究纳入至少 5 名成年患者(年龄≥18 岁),患有原发性局限性肾细胞癌,并接受 SBRT、射频消融、微波消融或冷冻消融治疗,且报告了局部控制结果。两名评审员独立筛选标题和摘要,然后由相同评审员独立评估符合条件研究的全文,如有分歧则通过讨论或咨询第三位评审员解决。使用标准化数据提取表从已发表报告中手动提取汇总估计值。主要终点为治疗开始后 1 年、2 年和 5 年的局部控制率。采用 DerSimonian 和 Laird 模型进行荟萃分析以总结局部控制率。使用漏斗图和 Egger 检验评估发表偏倚。我们还根据《不良事件通用术语标准》(第 5.0 版)和 Clavien-Dindo 并发症指数记录治疗后不良事件的发生频率和严重程度。本研究方案已前瞻性注册于 PROSPERO,注册号 CRD42024511840。
结果:我们共检索到 6668 条记录,其中 330 条通过全文审查进行评估,133 条纳入我们的系统评价与荟萃分析。符合条件的研究纳入了 8910 例患者的数据(平均年龄 67.9 岁[标准差 7.3],在 8018 例有可用数据的患者中,2518 例[31.4%]为女性,5500 例[68.6%]为男性)。SBRT 的局部控制率在 1 年时为 99%(95%CI: 97-100;I²=6%),2 年时为 97%(95%CI:95-99;I²=0%),5 年时为95%(95%CI:89-98;I²= 42%);射频消融的局部控制率 1 年时为96%(95%CI:94-98;I²=73%),2 年时为 95%(95%CI:92-98;I²=77%),5 年时为 92%(95%CI:88-96;I²=78%);微波消融的局部控制率 1 年时为 97%(95%CI:95-99;I²=74%),2 年时为 95%(95%CI:92-98;I²=77%),5 年时为 86%(95%CI:75-94;I²=66%);冷冻消融的局部控制率 1 年时为 95%(95%CI:93-96;I²=61%),2 年时为 94%(95%CI:91-96;I²=69%),5 年时为 90%(95%CI:87-93;I²=74%)。报告发生 3-4 级不良事件的患者比例,冷冻消融后为 3%(3726 例中有 121 例),射频消融后为 2%(2503例中有 39 例),微波消融后为 1%(2069 例中有 22 例),SBRT 后为 2%(612 例中有 11 例)。大多数研究(133 项中的 70 项[53%])的偏倚风险为中度,未观察到发表偏倚。
结论:所有研究的消融方法仍是肾细胞癌的有效治疗选择,这些发现支持将这些治疗方法与手术及监测一同纳入多学科讨论,以便为这些患者制定个体化治疗决策。未来的研究应致力于在更大的患者群体中开展随机对照试验,以进一步阐明这些治疗相关的长期肿瘤学结局和生存结果。
参考文献:
1. Yu EY, Rumble RB, Agarwal N, et al. Germline and Somatic Genomic Testing for Metastatic Prostate Cancer: ASCO Guideline [J]. J Clin Oncol. 2025 Jan 9:JCO2402608.
2. Naqvi SAA, Riaz IB, Bibi A, et al. Heterogeneity of the Treatment Effect with PARP Inhibitors in Metastatic Castration-resistant Prostate Cancer: A Living Interactive Systematic Review and Meta-analysis [J]. Eur Urol. 2025 Jan 22:S0302-2838(24)02760-X.
3. Ravi P, Kwak L, Acosta AM, et al.Long-term Outcomes and Prognostic Impact of Residual Cancer Burden After Intensified Neoadjuvant Therapy in High-risk Prostate Cancer [J]. Eur Urol. 2025 Feb 6:S0302-2838(25)00027-2.
4. Nikitas J, Jamshidian P, Tree AC, et al. The interplay between acute and late toxicity among patients receiving prostate radiotherapy: an individual patient data meta-analysis of six randomised trials [J]. Lancet Oncol. 2025 Jan 30:S1470-2045(24)00720-4.
5. de Bono JS, He M, Shi Z, et al. Final Overall Survival and Molecular Data Associated with Clinical Outcomes in Patients Receiving Ipatasertib and Abiraterone in the Phase 3 IPATential150 Trial [J]. Eur Urol. 2025 Jan 29:S0302-2838(24)02771-4.
6. Bedke J, Ghanem YA, Albiges L, et al. Updated European Association of Urology Guidelines on the Use of Adjuvant Immune Checkpoint Inhibitors and Subsequent Therapy for Renal Cell Carcinoma [J]. Eur Urol. 2025 Feb 3:S0302-2838(25)00026-0.
7. Motzer RJ, Porta C, Eto M, et al. Biomarker analyses from the phase III randomized CLEAR trial: lenvatinib plus pembrolizumab versus sunitinib in advanced renal cell carcinoma [J]. Ann Oncol. 2024 Dec 11:S0923-7534(24)04978-0.
8. Huang RS, Chow R, Benour A, et al. Comparative efficacy and safety of ablative therapies in the management of primary localised renal cell carcinoma: a systematic review and meta-analysis [J]. Lancet Oncol. 2025 Feb 5:S1470-2045(24)00731-9.



